Современные методы обеззараживания воды проект. Очистка и обеззараживание воды разными методами
Наиболее распространенными процессами водоочистки являются осветление и обеззараживание.
Помимо этого существуют специальные способы улучшения качества воды:
- умягчение воды (устранение катионов жесткости воды);
- обессоливание воды (снижение общей минерализации воды);
- обезжелезивание воды (снижение концентрации солей железа в воде);
- дегазация воды (удаление растворенных в воде газов);
- обезвреживание воды (удаление ядовитых веществ из воды);
- дезактивация воды (водоочистка от радиоактивных загрязнений).
Обеззараживание - завершающий этап процесса водоочистки. Цель - подавление жизнедеятельности содержащихся в воде болезнетворных микробов.
По способу воздействия на микроорганизмы методы обеззараживания воды подразделяются на химические, или реагентные; физические, или безреагентные, и комбинированные. В первом случае должный эффект достигается внесением в воду биологически активных химических соединений; безреагентные методы обеззараживания подразумевают обработку воды физическими воздействиями, а в комбинированных используются одновременно химическое и физическое воздействия.
К химическим способам обеззараживания питьевой воды относят ее обработку окислителями: хлором, озоном и т. п., а также ионами тяжелых металлов. К физическим - обеззараживание ультрафиолетовыми лучами, ультразвуком и т. д.
Наиболее распространенным химическим методом обеззараживания воды является хлорирование. Это объясняется высокой эффективностью, простотой используемого технологического оборудования, дешевизной применяемого реагента и относительной простотой обслуживания.
При хлорировании используют хлорную известь, хлор и его производные, под действием которых бактерии и вирусы, находящиеся в воде, погибают в результате окисления веществ.
Кроме главной функции - дезинфекции, благодаря окислительным свойствам и консервирующему эффекту последействия, хлор служит и другим целям - контролю за вкусовыми качествами и запахом, предотвращению роста водорослей, поддержанию в чистоте фильтров, удалению железа и марганца, разрушению сероводорода, обесцвечиванию и т.п.
По мнению экспертов, применение газообразного хлора приводит к потенциальному риску здоровью человека. Это связанно прежде всего с возможностью образования тригалометанов: хлороформа, дихлорбромметана, дибромхлорметана и бромоформа. Образование тригалометанов обусловлено взаимодействием соединений активного хлора с органическими веществами природного происхождения. Эти производные метана обладают выраженным канцерогенным эффектом, что способствуют образованию раковых клеток. При кипячении хлорированной воды в ней образуется сильнейший яд - диоксин.
Исследования подтверждают взаимосвязь хлора и его побочных продуктов с возникновением таких болезней, как рак органов пищеварительного тракта, печени, сердечные расстройства, атеросклероз, гипертония, различные виды аллергии. Хлор воздействует на кожу и волосы, а также разрушает белок в организме.
Одним из наиболее перспективных способов обеззараживания природной воды является использование гипохлорита натрия (NaClO), получаемого на месте потребления путем электролиза 2-4%-ных растворов хлорида натрия (поваренной соли) или природных минерализованных вод, содержащих не менее 50 мг/л хлорид-ионов.
Окислительное и бактерицидное действие гипохлорита натрия идентично растворенному хлору , кроме того, он обладает пролонгированным бактерицидным действием.
Основными достоинствами технологии обеззараживания воды гипохлоритом натрия является безопасность ее применения и значительное уменьшение воздействия на окружающую среду по сравнению с жидким хлором.
Наряду с достоинствами у обеззараживания воды гипохлоритом натрия, производимым на месте потребления, имеется и ряд недостатков, прежде всего - повышенный расход поваренной соли, обусловленный низкой степенью ее конверсии (до 10-20%). При этом остальные 80-90% соли в виде балласта вводятся с раствором гипохлорита в обрабатываемую воду, повышая ее солесодержание. Снижение же концентрации соли в растворе, предпринимаемое ради экономии, увеличивает затраты электроэнергии и расход анодных материалов.
Некоторые эксперты считают, что замена газообразного хлора гипохлоритом натрия или кальция для дезинфекции воды вместо молекулярного хлора не снижает, а значительно увеличивает вероятность образования тригалометанов. Ухудшение качества воды при применении гипохлорита, по их мнению, связано с тем, что процесс образования тригалометанов растянут во времени до нескольких часов, а их количество при прочих равных условиях тем больше, чем больше pH (величина, характеризующая концентрацию ионов водорода). Поэтому наиболее рациональным методом уменьшения побочных продуктов хлорирования является снижение концентрации органических веществ на стадиях очистки воды до хлорирования.
Альтернативные методы обеззараживания воды, связанные с использованием серебра, являются слишком дорогостоящими. Был предложен альтернативный хлорированию метод обеззараживания воды с помощью озона, но оказалось, что озон тоже вступает в реакцию со многими веществами в воде - с фенолом, и образовавшиеся в результате продукты еще токсичнее хлорфенольных. Кроме того, озон очень нестоек и быстро разрушается, поэтому его бактерицидное действие непродолжительно.
Из физических способов обеззараживания питьевой воды наибольшее распространение получило обеззараживание вод ы ультрафиолетовыми лучами, бактерицидные свойства которых обусловлены действием на клеточный обмен и, особенно, на ферментные системы бактериальной клетки. Ультрафиолетовые лучи уничтожают не только вегетативные, но и споровые формы бактерий, и не изменяют органолептических свойств воды. Основным недостатком метода является полное отсутствие последействия. Кроме того, этот метод требует больших капитальных вложений, чем хлорирование.
Материал подготовлен на основе информации открытых источников
Обеззараживание питьевой воды служит для создания надежного барьера на пути передачи водным путем возбудителей инфекционных болезней. Методы обеззараживания воды направлены на уничтожение патогенных и условно-патогенных микроорганизмов, чем обеспечивается эпидемическая безопасность воды.
Воду обеззараживают на конечном этапе очистки после осветления и обесцвечивания перед поступлением в резервуары чистой воды, которые одновременно выполняют функции контактных камер. Для обеззараживания воды применяют реагентные (химические) и безреагентные (физические) методы. Реагентные методы основаны на введении в воду сильных окислителей (хлорирование, озонирование, манганирование, обработка воды йодом), ионов тяжелых металлов и ионов серебра. К безреагентным относятся термическая обработка, ультрафиолетовое облучение, обработка ультразвуком, у-облучение, обработка током сверхвысокой частоты. Метод выбирают в зависимости от количества и качества исходной воды, методов ее предварительной очистки, требований к надежности обеззараживания, с учетом технико-экономических показателей, условий поставки реагентов, наличия транспорта, возможности автоматизации процесса.
Обеззараживание воды хлором и его соединениями. На сегодняшний день наиболее распространенным методом обеззараживания воды на водопроводных станциях остается хлорирование. Среди хлорсодержащих соединений, учитывая определенные гигиенические и технические преимущества, чаще всего используют жидкий хлор. Возможно также применение хлорной извести, кальция и натрия гипохлорита, хлора диоксида, хлораминов и др.
*Для использования в практике хозяйственно-питьевого водоснабжения допускаются лишь фторсодержащие соединения, прошедшие гигиеническую апробацию и включенные в "Перечень материалов и реагентов, разрешенных Главным санитарно-эпидемиологическим управлением Министерства здравоохранения СССР для применения в практике хозяйственно-питьевого водоснабжения (№ 3235-85)".*
Впервые в практике водоподготовки хлор был применен задолго до открытия Л. Пастером микробов, доказательства Р. Кохом этиологического значения патогенных микроорганизмов в развитии инфекционных болезней, окончательного осознания Т. Эшерихом микробиологической сущности водных эпидемий и бактерицидных свойств хлора. Применяли его с целью дезодорации воды, которая имела неприятный "септический"запах. Хлор оказался очень эффективным дезодорантом и, кроме того, после обработки воды хлором у людей значительно реже диагностировали кишечные инфекции. С началом хлорирования воды во многих странах Европы прекратились эпидемии брюшного тифа и холеры. Было высказано предположение, что причиной болезней были плохой запах и вкус воды, которые эффективно устранял хлор. Лишь со временем доказали микробную этиологию водных эпидемий кишечных инфекций и признали роль хлора в качестве обеззараживающего агента.
Для хлорирования воды применяют жидкий хлор, который хранится под давлением в специальной таре (баллонах), или вещества, содержащие активный хлор.
Хлорирование воды жидким хлором. Хлор (С12) при нормальном атмосферном давлении является газом зеленовато-желтого цвета, который в 1,5-
2,5 раза тяжелее воздуха, с резким и неприятным запахом, хорошо растворяется в воде, при повышении давления легко сжижается. Атомный вес хлора - 35,453, молекулярная масса - 70,906 г/моль. Хлор может находиться в трех агрегатных состояниях: твердом, жидком и газообразном.
Хлор на водопроводные станции для обеззараживания воды доставляют жидким в баллонах под давлением. Хлорирование осуществляют при помощи хлораторов. В них готовят раствор хлора, который вводят непосредственно в трубопровод, по которому вода поступает в РЧВ. Используют хлораторы Л.А. Кульского (рис. 20), вакуумные хлораторы ЛОНИИ-100, Ж-10, ЛК-12, ХВ-11. Принципиальная схема хлоратора ЛОНИИ-100 изображена на рис. 21.
При подключении баллона к хлоратору жидкий хлор испаряется. Газообразный хлор очищается в баллоне и на фильтре, и после снижения его давления с помощью редуктора до 0,001- 0,02 МПа его смешивают в смесителе с водой. Из смесителя концентрирован-
Рис. 21. Технологическая схема типичной хлораторной на 3 кг/ч: 1 - весы платформные; 2 - стояки с баллонами; 3 - улавливатель загрязнений; 4 - хлораторы ЛОНИИ-100; 5 - эжекторы
Ный раствор всасывается эжектором и подается в трубопровод. Хлораторы типа ЛК, конструкция которых проще, а точность ниже используют для станций больших мощностей. Эти хлораторы не требуют предварительной очистки хлора, не так точны в дозировании, но могут подавать хлорную воду на высоту 20- 30 м. После же эжектора от ЛОНИИ-100 напор составляет лишь 1-2 м. Во время растворения хлора в воде происходит его гидролиз с образованием хлоридной (соляной) и гипохлоритной (или хлорноватистой) кислот:
С12+ Н20 ^ HCl + НС10.
Хлорноватистая кислота НС10 является слабой одноосновной нестойкой кислотой, которая легко диссоциирует, образуя гипохлорит-ион (СЮ~):
НСЮ ^ Н+ + СЮ".
Степень диссоциации хлорноватистой кислоты зависит от pH воды. При pH
Кроме того, хлорноватистая кислота распадается с образованием атомарного кислорода, который также является сильным окислителем:
НСЮ It HCl + О".
*Активным хлором называется такой, который способен при pH 4 выделять эквивалентное количество йода из водных растворов калия йодида. Различают свободный (молекулярный хлор, хлорноватистая кислота, гипохлорит-ион) и связанный (хлор, входящий в состав органических и неорганических моно- и дихлораминов) активный хлор.*
Раньше считали, что именно этот атомарный кислород оказывает бактерицидное действие. Сегодня доказано, что обеззараживающий эффект жидкого хлора, а также хлорной извести, кальция и натрия гипохлоритов, двухтретиос-новной соли кальция гипохлорита обусловлен окислителями, которые образуются в воде при растворении хлорсодержащих соединений, причем прежде всего - действием гипохлоритной кислоты, а затем - гипохлоритного аниона и наконец атомарного кислорода.
Хлорирование воды гипохлоритами (солями хлорноватистой кислоты) проводят на водопроводных станциях низкой мощности. Гипохлориты также используют для длительного обеззараживания воды в шахтных колодцах при помощи керамических патронов, для обеззараживания воды в полевых условиях, в том числе с использованием тканево-угольных фильтров и др.
Для дезинфекции питьевой воды используют кальция гипохлорит Са(ОС1)2. В процессе его растворения в воде происходит гидролиз с образованием хлорноватистой кислоты и дальнейшей ее диссоциацией:
Са(ОС1)2 + 2Н20 = Са(ОН)2 + 2НСЮ,
Нею -?. н+ + cicr.
В зависимости от способа производства кальция гипохлорит может содержать от 57-60% до 75-85% активного хлора. Вместе с чистым гипохлоритом для обеззараживания воды используют смесь кальция гипохлорита с другими солями (NaCl, СаС12). Такие смеси содержат до 60-75% чистого гипохлорита.
На станциях с расходом активного хлора до 50 кг/сут можно использовать для обеззараживания воды натрия гипохлорит (NaCIO 5Н20). Этот кристаллогидрат получают из раствора натрия хлорида (NaCl) электролитическим способом.
Натрия хлорид в воде диссоциирует с образованием катиона натрия и аниона хлора:
NaCl ^ Na+ + СГ
Во время электролиза на аноде происходит разряжение ионов хлора и образуется молекулярный хлор:
2СГ -» С12 + 2е.
Образовавшийся хлор растворяется в электролите:
С12+Н2О^НС1 + НСЮ,
С12+ОН-^СІ+НСЮ.
На катоде происходит разряд молекул воды:
Н20 + е -> ОН- + Н+.
Атомы водорода после рекомбинации в молекулярный водород выделяются из раствора в виде газа. Гидроксильные анионы ОН", оставшиеся в воде, реагируют с катионами натрия Na+, вследствие чего образуется NaOH. Натрия гидроксид взаимодействует с хлорноватистой кислотой с образованием натрия гипохлорита:
NaOH + НС10 -> NaOCI + Н20.
Рис. 22. Технологическая схема электролитического получения натрия гипохлорита: 1 - растворный бак; 2 - насос; 3 - распределительный тройник; 4 - рабочий бак; 5 - дозатор; 6 - электролизер с графитовыми электродами; 7 - бак-накопитель натрия гипохлорита; 8 - зонт вытяжной вентиляции
Натрия гипохлорит в значительной мере диссоциирует с образованием СЮ", который обладает высокой антимикробной активностью:
NaCIO ^ Na+ + СЮ",
Сю- + н+;^нсю.
Электролизерные установки разделяют на проточные и порционные. В их состав входят электролизеры, разнотипные баки. Принципиальная схема порционной установки изображена на рис. 22. Раствор натрия хлорида 10% концентрации подают в бак постоянного уровня, откуда он вытекает с постоянным расходом. После заполнения бачка-дозатора срабатывает сифон и сливает определенный объем раствора в электролизер. Под воздействием электрического тока в электролизере образуется натрия гипохлорит. Новые порции раствора соли выталкивают натрия гипохлорит в расходный бак, из которого он дозируется насосом-дозатором. Бак-накопитель должен вмещать объем натрия гипохлорита не менее чем на 12 ч.
Преимуществом получения натрия гипохлорита электролитическим методом в месте употребления является то, что отпадает необходимость в транспортировке и хранении токсического сжиженного хлора. Среди недостатков можно назвать значительные энергозатраты.
Обеззараживание воды прямым электролизом. Метод состоит в прямом электролизе пресной воды, в которой природное содержание хлоридов не ниже 20 мг/л, а жесткость - не выше 7 мг-экв/л. Применяют на водопроводных станциях мощностью до 5000 м3/сут. Вследствие прямого электролиза на аноде происходит разряжение находящихся в воде хлорид-ионов и образуется молекулярный хлор, который гидролизуется с образованием хлорноватистой кислоты:
2СГ ^ С12 + 2е, С12 + Н2О^НС1 + НСЮ.
Во время обработки электролизом воды с pH в пределах 6-9 главными дезинфекционными агентами являются хлорноватистая (гипохлоритная) кислота НСЮ, гипохлорит-анион С10~ и монохлорамины NH2C1, которые образуются вследствие реакции между НСЮ и аммонийными солями, содержащимися в природной воде. Одновременно во время обработки воды электролитическим методом на микроорганизмы действует электрическое поле, в котором они находятся, что усиливает бактерицидный эффект.
Обеззараживание воды хлорной известью применяют на малых водопроводных станциях (производительностью до 3000 м3/сут), предварительно приготовив раствор. Хлорной известью также заполняют керамические патроны для обеззараживания воды в шахтных колодцах или на локальных водопроводах.
Хлорная известь - белый порошок с резким запахом хлора и сильными окисляющими свойствами. Это смесь кальция гипохлорита и кальция хлорида. Получают хлорную известь из известняков. Кальция карбонат при температуре 700 °С распадается с образованием негашеной извести (кальция оксид), которая после взаимодействия с водой превращается в гашеную известь (кальция гидроксид). При взаимодействии хлора с гашеной известью образуется хлорная известь:
СаСОз ^ СаО + С02,
СаО + Н20 = Са(ОН)2,
2Са(ОН)2 + 2С12 = Са(ОС1)2 + СаС12+ 2Н20 или
2Са(ОН)2 + 2С12= 2СаОС12 + 2Н20.
Основную составную часть хлорной извести выражают формулой:
Технический продукт содержит не более 35% активного хлора. В процессе хранении хлорная известь частично разлагается. То же происходит с кальция гипохлоритом. Свет, влажность и высокая температура ускоряют потерю активного хлора. Хлорная известь теряет приблизительно 3-4% активного хлора в месяц вследствие реакций гидролиза и разложения на свету. Во влажном помещении хлорная известь разлагается, образуя хлорноватистую кислоту:
2СаОС12 + С02 + Н20 = СаС03 + СаС12 + 2НСЮ.
Поэтому перед использованием хлорной извести и кальция гипохлорита проверяют их активность - выраженное в процентах содержание активного хлора в хлорсодержащем препарате.
Бактерицидным действием хлорная известь, так же, как и гипохлориты, обязана группе (ОСГ), которая в водной среде образует хлорноватистую кислоту:
2СаОС12 + 2Н20 -> СаС12 + Са(ОН)2 + 2НС10.
Хлора диоксид (ClOJ - газ желто-зеленого цвета, легко растворяется в воде (при температуре 4 °С в 1 объеме воды растворяется 20 объемов газообразного СЮ2). Не гидролизует. Его целесообразно применять в случае, если особенности природной воды являются неблагоприятными для эффективного обеззараживания хлором, например, при высоких значениях pH или в присутствии аммиака. Однако получение хлора диоксида является сложным процессом, который требует специального оборудования, квалифицированного персонала, дополнительных финансовых затрат. Кроме того, хлора диоксид взрывоопасен, что требует строгого соблюдения требований техники безопасности. Указанное ограничивает использование хлора диоксида для обеззараживания воды на хозяйственно-питьевых водопроводах.
К хлорсодержащим препаратам относятся и хлорамины (неорганические и органические), которые в практике водоподготовки используют ограничено, но применяют как обеззараживающие агенты во время проведения мероприятий по дезинфекции, в частности в лечебно-профилактических учреждениях. Неорганические хлорамины (монохлорамины NH2C1 и дихлорамины NHC12) образуются при взаимодействии хлора с аммиаком или аммонийными солями:
NH3 + CI2 = NH2CI + HCI,
NH2CI + CI2 = NHCI2 + HCl.
Вместе с неорганическими соединениями хлора для обеззараживания используют и органические хлорамины (RNHC1, RNC12). Их получают в процессе взаимодействия хлорной извести с аминами или их солями. При этом один или два атома водорода аминной группы замещаются хлором. Разные хлорамины содержат 25-30% активного хлора.
Процесс обеззараживания воды хлорсодержащими препаратами происходит в несколько стадий:
1. Гидролиз хлора и хлорсодержащих препаратов:
С12 + Н20 = HCl + НС10;
Са(ОС1)2 +2Н20 = Са(ОН)2+ 2НС10;
2СаОС12 + 2Н20 = Са(ОН)2 + СаС12 + 2НС10.
2. Диссоциация хлорноватистой кислоты.
При pH ~ 7,0 НС10 диссоциирует: НС10
3. Диффузия в бактериальную клетку молекулы НС10 и иона СЮ".
4. Взаимодействие обеззараживающего агента с энзимами микроорганизмов, которые окисляются хлорноватистой кислотой и гипохлорит-ионом.
Активный хлор (НСЮ и СЮ") сначала диффундирует внутрь бактериальной клетки, а затем вступает в реакцию с ферментами. Наибольшее бактерицидное и вирулицидное действие оказывает недиссоциированная хлорноватистая кислота (НСЮ). Скорость процесса обеззараживания воды определяется кинетикой диффузии хлора внутрь бактериальной клетки и кинетикой отмирания клеток в результате нарушения метаболизма. С повышением концентрации хлора в воде, ее температуры и с переходом хлора в недиссоциированную форму легко диффундируемой хлорноватистой кислоты общая скорость процесса дезинфекции повышается.
Механизм бактерицидного действия хлора состоит в окислении органических соединений бактериальной клетки: коагуляции и повреждении ее оболочки, угнетении и денатурации ферментов, обеспечивающих обмен веществ и энергии. Наиболее всего повреждаются тиоловые ферменты, содержащие SH-группы, которые окисляются хлорноватистой кислотой и ионом гипохло-рита. Среди тиоловых ферментов активнее всего угнетается группа дегидроге-наз, которые обеспечивают дыхание и энергетический обмен бактериальной клетки1. Под влиянием хлорноватистой кислоты и гипохлорит-иона угнетаются дегидрогеназы глюкозы, этилового спирта, глицерина, янтарной, глютами-новой, молочной, пировиноградной кислот, формальдегида и др. Угнетение де-гидрогеназ приводит к торможению процессов окисления на начальных этапах. Последствием этого является как торможение процессов размножения бактерий (бактериостатическое действие), так и их гибель (бактерицидное действие).
Механизм действия активного хлора на вирусы состоит из двух фаз. Сначала происходят адсорбция хлорноватистой кислоты и гипохлорит-иона на оболочке вируса и проникновение через нее, а затем - инактивация ими РНК или ДНК вируса.
С повышением значения pH бактерицидность хлора в воде снижается. Например, для уменьшения количества бактерий в воде на 99% при дозе свободного хлора 0,1 мг/л продолжительность контакта увеличивается с 6 до 180 мин при повышении pH соответственно с 6 до 11. Следовательно воду целесообразно обеззараживать хлором при низких значениях pH, то есть до введения щелочных реагентов.
Наличие в воде органических соединений, способных к окислению, неорганических восстановителей, а также коллоидных и взвешенных веществ, обволакивающих микроорганизмы, приводит к замедлению процесса обеззараживания воды.
Взаимодействие хлора с компонентами воды - сложный и многостадийный процесс. Небольшие дозы хлора полностью связываются органическими веществами, неорганическими восстановителями, взвешенными частицами, гуминовыми веществами и микроорганизмами воды. Для надежного обеззараживающего эффекта воды после ее хлорирования необходимо определять остаточные концентрации свободного или связанного активного хлора.
*Энергетический метаболизм у бактерий происходит в мезосомах - аналогах митохондрий.*
Рис. 23. График зависимости величины и вида остаточного хлора от введенной дозы хлора
На рис. 23 приведена зависимость между дозой введенного хлора и остаточным хлором при наличии в воде аммиака или аммонийных солей. При хлорировании воды, не содержащей аммиака или других азотсодержащих соединений", с увеличением количества внесенного в воду хлора возрастает содержание в ней остаточного свободного хлора. Но картина меняется при наличии в воде аммиака, аммонийных солей и других азотсодержащих соединений, которые являются составной частью природной воды или искусственно вносятся в нее. При этом хлор и хлорные агенты взаимодействуют с присутствующим в воде аммиаком, аммонийными и органическими солями, содержащими аминогруппы. Это приводит к образованию моно- и дихлораминов, а также чрезвычайно нестойких трихлораминов:
NH3 + Н20 = NH4OH;
С12 + Н20 = НС10 + HCl;
НСЮ + NH4OH = NH2C1 + Н20;
НСЮ + NH2C1 = NHC12+ H20;
НСЮ + NHC12 = NC13 + Н20.
Хлорамины представляют собой связанный активный хлор, обладающий бактерицидным действием, которое в 25-100 раз меньше, чем у свободного хлора. Кроме того, в зависимости от pH воды изменяется соотношение между моно- и дихлораминами (рис. 24). При низких значениях pH (5-6,5) преимущественно образуются дихлорамины, а при больших значениях pH (больше 7,5) - монохлорамины, бактерицидное действие которых в 3-5 раз слабее, чем дихлораминов. Бактерицидность неорганических хлораминов в 8-10 раз выше, чем хлорпроизводных органических аминов и иминов. При добавлении к воде невысоких доз хлора при молярном соотношении С12: NH*
*Безаммиачной воды в природе нет. Ее можно приготовить лишь в лабораторных условиях из дистиллированной воды.*
накапливается остаточный связанный с аминами хлор. При увеличении дозы хлора образуется больше хлораминов и концентрация остаточного связанного хлора повышается до максимума (точка А).
При дальнейшем увеличении дозы хлора молярное соотношение введенного хлора и иона NH *, содержащего в воде, становится больше единицы. При этом моно-, ди- и, особенно, трихлорамины окисляются избыточным хлором в соответствии с приведенными реакциями:
NHC12 + NH2C1 + НСЮ -> N20 + 4НС1;
NHC12 + Н20 -> NH(OH)Cl + HCl;
NH(OH)Cl + 2HC10 -> HN03 + ЗНС1;
NHC12 + HCIO -> NC13 + H20;
4NH2C1 + 3C12 + H20 = N2 + N20 + 10HC1;
IONCI3 + CI2 + 16H20= N2 + 8N02 + 32HCI.
При молярном соотношения Cl2: NH \ до 2 (10 мг Cl2 на 1 мг N2 в виде NH \) вследствие окисления хлораминов избыточным хлором количество остаточного связанного хлора в воде резко снижается (отрезок III) до минимальной точки (точки В), которая называется точкой перелома. Графически она имеет вид глубокого провала на кривой остаточного хлора (см. рис. 23).
При дальнейшем увеличении дозы хлора после точки перелома концентрация остаточного хлора в воде вновь начинает постепенно возрастать (отрезок IV на кривой). Этот хлор не связан с хлораминами, носит название свободного остаточного (активного) хлора и имеет наивысшую бактерицидную активность. Действует на бактерии и вирусы подобно активному хлору при отсутствии в воде аммиака и аммонийных соединений.
Как свидетельствуют данные исследований, воду можно обеззараживать двумя дозами хлора: до- и послепереломной. Однако при хлорировании допереломной дозой вода обеззараживается за счет действия хлораминов, а при хлорировании послепереломной - свободного хлора.
Во время обеззараживания воды добавляемый хлор расходуется как на взаимодействие с микробными клетками и вирусами, так и на окисление органических и минеральных соединений (мочевины, мочевой кислоты, креатини-на, аммиака, гуминовых веществ, солей двухвалентного железа, аммонийных солей, карбаматов и др.), которые содержатся в воде во взвешенном и растворенном состоянии. Количество хлора, поглощенное примесями воды (органическими веществами, неорганическими восстановителями, взвешенными частицами, гуминовыми веществами и микроорганизмами), называется хлорпог-лощаемостью воды (отрезок I на кривой). Поскольку природные воды имеют различный состав, то и величина хлорпоглощаемости у них неодинакова. Таким образом, хлорпоглощаемость - это количество активного хлора, которое поглощается взвешенными частицами и расходуется на окисление бактерий, органических и неорганических соединений, содержащихся в 1 л воды.
Рассчитывать на успешное обеззараживание воды можно лишь при наличии некоторого избытка хлора по отношению к количеству, которое поглощается бактериями и различными соединениями, содержащимися в воде. Эффективной является доза активного хлора, равная суммарному количеству поглощенного и остаточного хлора. С присутствием в воде остаточного хлора (или, как его еще называют, избыточного) связано представление об эффективности обеззараживания воды.
При хлорировании воды жидким хлором, кальция и натрия гипохлоритами, хлорной известью 30-минутный контакт обеспечивает надежный обеззараживающий эффект при концентрации остаточного хлора не меньше 0,3 мг/л. Но при хлорировании с преаммонизацией контакт должен быть на протяжении 1-2 ч, а эффективность обеззараживания будет гарантированной при наличии остаточного связанного хлора в концентрации не менее 0,8 мг/л.
Хлор и хлорсодержащие соединения в значительной мере влияют на органолептические свойства питьевой воды (запах, привкус), а в определенных концентрациях раздражают слизистые оболочки ротовой полости и желудка. Предельная концентрация остаточного хлора, при которой питьевая вода не приобретает хлорного запаха и привкуса, установлена для свободного хлора на уровне 0,5 мг/л, а для связанного - 1,2 мг/л. По токсикологическим признакам предельной концентрацией активного хлора в питьевой воде является 2,5 мг/л".
Следовательно, для обеззараживания воды необходимо добавить такое количество хлорсодержащего препарата, чтобы после обработки вода содержала 0,3-0,5 мг/л остаточного свободного или 0,8-1,2 мг/л остаточного связанного хлора. Такой избыток активного хлора не ухудшает вкуса воды, не вредит здоровью, но гарантирует ее надежное обеззараживание.
Таким образом, для эффективного обеззараживания к воде добавляют дозу активного хлора, равную сумме хлорпоглощаемости и остаточного активного хлора. Эта доза называется хлорпотребностью воды.
Хлорпотребностъ воды - это количество активного хлора (в миллиграммах), необходимое для эффективного обеззараживания 1 л воды и обеспечивающее содержание остаточного свободного хлора в пределах 0,3-0,5 мг/л после 30-минутного контакта с водой, или количество остаточного связанного хлора в пределах 0,8-1,2 мг после 60-минутного контакта. Содержание остаточного
*Предельная концентрация хлора диоксида в питьевой воде - не выше 0,5 мг/л, лимитирующий показатель водного действия - органолептический.*
Активного хлора контролируют после резервуаров чистой воды перед подачей в водопроводную сеть. Поскольку хлорпоглощаемость воды зависит от ее состава и является неодинаковой для воды из разных источников, то в каждом случае хлорпотребность определяют экспериментально путем пробного хлорирования. Ориентировочно хлорпотребность осветленной и обесцвеченной коагуляцией, отстаиванием и фильтрацией речной воды колеблется в пределах 2-3 мг/л (иногда - до 5 мг/л), воды подземных межпластовых вод - в пределах 0,7-1 мг/л.
Факторы, влияющие на процесс хлорирования воды, связаны с: 1) биологическими особенностями микроорганизмов; 2) бактерицидными свойствами хлорсодержащих препаратов; 3) состоянием водной среды; 4) с условиями, в которых осуществляется обеззараживание.
Известно, что споровые культуры во много раз более устойчивы, чем вегетативные формы к действию дезинфицирующих средств. Энтеровирусы более стойкие, чем кишечные бактерии. Сапрофитные микроорганизмы более резистентны, чем патогенные. При этом среди патогенных микроорганизмов наиболее чувствительными к хлору являются возбудители брюшного тифа, дизентерии, холеры. Возбудитель паратифа В более стойкий к действию хлора. Кроме того, чем выше инициальная контаминация воды микроорганизмами, тем ниже при одинаковых условиях эффективность обеззараживания.
Бактерицидная активность хлора и его соединений связана с величиной его окислительно-восстановительного потенциала. Окислительно-восстановительный потенциал возрастает при одинаковых концентрациях в ряду: хлорамин -> хлорная известь -> хлор -» хлора диоксид.
Эффективность хлорирования зависит от свойств и состава водной среды, а именно: от содержания взвешенных веществ и коллоидных соединений, концентрации растворенных органических соединений и неорганических восстановителей, pH воды, ее температуры.
Взвешенные вещества и коллоиды препятствуют воздействию дезинфицирующего агента на микроорганизмы, находящиеся в толще частицы, поглощают активный хлор вследствие адсорбции и химического связывания. Влияние на эффективность хлорирования органических соединений, растворенных в воде, зависит как от их состава, так и от свойств хлорсодержащих препаратов. Так, азотсодержащие соединения животного происхождения (белки, аминокислоты, амины, мочевина) активно связывают хлор. Соединения, не содержащие азота (жиры, углеводы), слабее реагируют с хлором. Поскольку наличие в воде взвешенных веществ, гуминовых и других органических соединений снижает эффект хлорирования, для надежного обеззараживания мутные и повышенной цветности воды предварительно осветляют и обесцвечивают.
При снижении температуры воды до 0-4 °С уменьшается бактерицидный эффект хлора. Эта зависимость особенно заметна в опытах с высокой инициальной контаминацией воды и в случае хлорирования ее невысокоми дозами хлора. В практике работы водопроводных станций, если загрязнение воды источника отвечает требованиям Госстандарта 2761-84 "Источники централизованного хозяйственно-питьевого водоснабжения. Гигиенические, технические требования и контроль за качеством", снижение температуры заметно не влияет на эффективность обеззараживания.
Механизм влияния pH воды на ее обеззараживание хлором связан с особенностями диссоциации хлорноватистой кислоты: в кислой среде равновесие смещается в сторону молекулярной формы, в щелочной - ионной. Хлорноватистая кислота в недиссоциированной молекулярной форме лучше проникает через оболочки в середину бактериальной клетки, чем гидратированные ионы гипохлорита. Поэтому в кислой среде процесс обеззараживания воды ускоряется.
На бактерицидный эффект хлорирования значительно воздействуют доза реагента и продолжительность контакта: бактерицидный эффект возрастает при повышении дозы и увеличении продолжительности действия активного хлора.
Способы хлорирования воды. Существует несколько способов хлориро-. вания воды с учетом характера остаточного хлора, выбор которых определяется особенностями состава обрабатываемой воды. Среди них: 1) хлорирование послепереломными дозами; 2) обычное хлорирование или хлорирование по хлорпотребности; 3) суперхлорирование; 4) хлорирование с преаммонизацией. В первых трех вариантах воду обеззараживают свободным активным хлором. При хлорировании с преаммонизацией бактерицидный эффект обусловлен действием хлораминов, т. е. связанного активного хлора. Кроме того, применяются комбинированные способы хлорирования.
Хлорирование послепереломными дозами предусматривает, что после 30 мин контакта в воде будет присутствовать свободный активный хлор. Дозу хлора подбирают таким образом, чтобы она была несколько выше той дозы, при которой образуется перелом на кривой остаточного хлора, т. е. в диапазоне IV (см. рис. 23). Подобранная таким способом доза обусловливает появление в воде остаточного свободного хлора в наименьшем количестве. Этот метод отличается тщательным подбором дозы. Он дает стойкий и надежный бактерицидный эффект, препятствует появлению запахов в воде.
Обычное хлорирование (хлорирование по хлорпотребности) является наиболее распространенным способом обеззараживания питьевой воды при централизованном хозяйственно-питьевом водоснабжении. Хлорирование по хлорпотребности проводится такой послепереломной дозой, которая через 30 мин контакта обеспечивает присутствие в воде остаточного свободного хлора в пределах 0,3-0,5 мг/л.
Поскольку природные воды существенно отличаются по составу и поэтому имеют различную хлорпоглощаемость, хлорпотребность определяют экспериментально путем опытного хлорирования воды, подлежащей обеззараживанию. Помимо правильного выбора дозы хлора, обязательным условием эффективного обеззараживания воды является тщательное смешивание и время экспозиции, т. е. время контакта хлора с водой (не менее 30 мин).
Как правило, на водопроводных станциях хлорирование по хлорпотребности проводят после осветления и обесцвечивания воды. Хлорпотребность такой воды колеблется в пределах 1-5 мг/л. Оптимальную дозу хлора вводят в воду сразу после фильтрации перед РЧВ.
Исходя из хлорпотребности, можно проводить и двойное хлорирование, при котором первый раз хлор подают в смеситель перед камерой реакции, а второй - после фильтров. При этом экспериментально определенную оптимальную дозу хлора не изменяют. Хлор при введении в смеситель перед камерой реакции улучшает коагуляцию и обесцвечивание воды, чем дает возможность снизить дозу коагулянта. Кроме того, он угнетает рост микрофлоры, которая загрязняет песок на фильтрах. Общие расходы хлора при двойном хлорировании практически не увеличиваются и остаются почти такими же, как и при одноразовом.
Двойное хлорирование заслуживает широкого применения. К нему следует обращаться в тех случаях, когда загрязнение речной воды сравнительно высокое или подвержено частым колебаниям. Двойное хлорирование повышает санитарную надежность обеззараживания воды.
Суперхлорирование (перехлорирование) является способом обеззараживания воды, при котором используются повышенные дозы активного хлора (5-20 мг/л). Эти дозы фактически являются послепереломными. К тому же они значительно превышают хлорпотребность природной воды и обусловливают наличие в ней высоких (свыше 0,5 мг/л) концентраций остаточного свободного хлора. Поэтому метод суперхлорирования не требует предварительного определения хлорпотребности воды и тщательного подбора дозы активного хлора, однако после обеззараживания необходимо удалить избыточный свободный хлор.
Суперхлорирование используют при особой эпидемиологической обстановке, при невозможности определить хлорпотребность воды и обеспечить достаточное время контакта хлора с водой, а также с целью предупреждения появления запахов воды и борьбы с ними. Этот метод удобен в военно-полевых условиях, при чрезвычайных ситуациях.
Суперхлорирование эффективно обеспечивает надежное обеззараживание даже мутной воды. От высоких доз активного хлора гибнут устойчивые к действию дезинфектантов возбудители, такие, как риккетсии Бернетта, цисты дизентерийной амебы, микобактерии туберкулеза и вирусы. Но даже такие дозы хлора не могут надежно обеззаразить воду от спор сибирской язвы и яиц гельминтов.
При суперхлорировании остаточный свободный хлор в обеззараженной воде значительно превышает 0,5 мг/л, что делает воду непригодной для употребления вследствие ухудшения ее органолептических свойств (резкий запах хлора). Поэтому возникает необходимость в освобождении ее от избытка хлора. Такой процесс называется дехлорированием. Если избыток остаточного хлора невелик, его можно удалить путем аэрации. В остальных случаях воду очищают, фильтруя через слой активированного угля или с помощью химических методов, таких, как обработка натрия гипосульфитом (тиосульфатом), натрия бисульфитом, сернистым ангидридом (серы диоксидом), железа сульфатом. На практике применяют преимущественно натрия гипосульфит (тиосульфат) - Na2S203 5Н20. Количество его рассчитывают в зависимости от количества избыточного хлора, исходя из следующей реакции:
Na2S203 + С12+ Н20 = Na2S04 + 2HCI + si.
Согласно приведенной реакции связывания между активным хлором и натрия гипосульфитом при мольном соотношении 1:1, на 0,001 г хлора используется 0,0035 г кристаллогидрата натрия гипосульфита, или на 1 мг хлора - 3,5MrNa2S203-5H20.
Хлорирование с преаммонизацией. Метод хлорирования в преаммонизацией используется:
1) с целью предотвращения появления неприятных специфических запахов, которые возникают после хлорирования воды, содержащей фенол, бензол и этилбензол;
2) для предотвращения образования канцерогенных веществ (хлороформ и др.) при хлорировании питьевой воды, содержащей гуминовые кислоты, углеводороды метанового ряда;
3) для снижения интенсивности запаха и привкуса хлора, особенно ощутимого в летнее время;
4) для экономии хлора при высокой хлорпоглощаемости воды и отсутствии запахов, привкусов и высокого бактериального загрязнения.
Если природная вода содержит фенолы (например, вследствие загрязнения водоемов сточными водами промышленных предприятий) даже в незначительных количествах1, то при обеззараживании хлорсодержащими соединениями, которые гидролизуются с образованием хлорноватистой кислоты, свободный активный хлор сразу же взаимодействует с фенолом, образуя хлорфенолы, которые даже в небольших концентрациях придают воде птечный привкус и запах. В то же время связанный активный хлор - хлораминный, имея более низкий окислительно-восстановительный потенциал, не взаимодействует с фенолом с образованием хлорфе-нолов, и поэтому во время обеззараживания не ухудшаются органолептические свойства воды. Аналогично свободный активный хлор способен взаимодействовать с углеводородами метанового ряда с образованием тригалометанов (хлороформа, дибромхлорметана, дихлорбромметана), являющихся канцерогенами. Предотвратить их образование можно, обеззараживая воду связанным активным хлором.
При хлорировании с преаммонизацией в воду, которую обеззараживают, сначала добавляют раствор аммиака2 или его солей, а через 1-2 мин вводят хлор. Вследствие этого в воде образуются хлорамины (монохлорамины NH2C1 и дихлорамины NHC12), которые обладают бактерицидным действием. Химические реакции образования хлораминов приведены на с. 170.
Соотношение образующихся веществ зависит от pH, температуры и количества реагирующих соединений. Эффективность хлорирования с преаммонизацией зависит от соотношения NH3 и С12, причем используют дозы этих реагентов в пропорциях 1:2, 1:4, 1:6, 1:8. Для воды каждого источника водоснабжения необходимо подбирать наиболее эффективное соотношения. Скорость обеззараживания воды хлораминами ниже, чем скорость дезинфекции свободным хлором, поэтому продолжительность дезинфекции воды в случае хлорирования с преаммонизацией должна быть не меньше 2 ч. Особенности бактерицидного действия хлораминов, а также их способность не образовывать хлорпроизводных, имеющих специфические запахи, объясняется их значитель-
*ПДК фенола в воде 0,001 мг/л, лимитирующий показатель - органолептический (запах), 4-й класс опасности.*
*Для введения аммиака в воду удобнее всего использовать вакуумные хлораторы.*
Но меньшей окислительной активностью, поскольку окислительно-восстановительный потенциал хлораминов значительно ниже, чем у хлора.
Кроме преаммонизации (введение аммиака за 1-2 мин до введения хлора), иногда применяют постаммонизацию, когда аммиак вводят после хлора непосредственно в резервуары с чистой водой. Благодаря этому хлор фиксируется дольше, чем достигается увеличение продолжительности его действия.
Комбинированные способы хлорирования воды. Кроме рассмотренных методов хлорирования воды, предложен ряд комбинированных, когда вместе с хлорсодержащими соединениями используют еще один химический или физический дезинфицирующий агент, что повышает эффект обеззараживания. Хлорирование можно комбинировать с обработкой воды солями серебра (хлор-серебряный метод), калия перманганатом (хлорирование с манганированием), озоном или ультрафиолетом, ультразвуком и т. п.
Хлорирование с манганированием (с добавлением раствора КМп04) используют при необходимости усиления окислительного и бактерицидного действия хлора, так как калия перманганат более сильный окислитель. Способ следует применять при наличии в воде запахов и привкусов, которые обусловлены органическими веществами, водорослями. При этом калия перманганат вводят до хлорирования. Добавлять КМп04 следует перед отстойниками в дозах 1-5 мг/л или перед фильтрами в дозе 0,08 мг/л. Восстанавливаясь до нерастворимого в воде Мп02, он полностью задерживается в отстойниках и на фильтрах.
Хлорсеребряный метод используют на судах речного флота (на установках КВУ-2 и УКВ-0,5). Он обеспечивает усиленное обеззараживание воды и ее консервацию на длительный срок (до 6 мес) при добавлении ионов серебра в количестве 0,05-0,1 мг/л.
Кроме того, хлорсеребряный метод используют для обеззараживания воды в плавательных бассейнах, где необходимо по мере возможности снизить дозу хлора. Это возможно потому, что бактерицидное действие обеспечивается в пределах суммарного эффекта доз хлора и серебра.
Бактерицидное, вирулицидное и окислительное действие хлора может быть усилено за счет одновременного воздействия ультразвуком, ультрафиолетовым излучением, постоянным электрическим током.
Пробы воды отбирают после резервуаров чистой воды перед подачей в водопроводную сеть. Контроль эффективности хлорирования по остаточному активному хлору осуществляют ежечасно, то есть 24 раза в сутки. Хлорирование считается эффективным, если содержание остаточного свободного хлора находится в пределах 0,3-0,5 мг/л через 30 мин контакта, или содержание остаточного связанного хлора составляет 0,8-1,2 мг/л через 60 мин контакта.
По микробиологическим показателям эпидемической безопасности воду после РЧВ исследуют дважды в сутки, то есть 1 раз в 12 ч. В воде после обеззараживания определяют общее микробное число и индекс БГКП (коли-индекс). Обеззараживание воды считается эффективным, если коли-индекс не превышает 3, а общее микробное число - не более 100.
Отрицательные последствия хлорирования воды для здоровья населения. В результате реакции хлора с гуминовыми соединениями, продуктами жизнедеятельности гидробионтов и некоторыми веществами промышленного происхождения образуются десятки новых чрезвычайно опасных галоформ-ных соединений, в том числе канцерогены, мутагены и высокотоксичные вещества с ПДК на уровне сотых и тысячных миллиграмма на 1 л. В табл. 3 и 5 (см. с. 66, 67, 101) приведены некоторые галогенсодержащие соединения, особенности их действия на организм человека, гигиенические нормативы в питьевой воде. Индикаторами этой группы являются тригалометаны: хлоро- и бро-моформ, дибромхлорметан, бромдихлорметан. В обеззараженной питьевой воде и воде горячего водоснабжения чаще всего и в более высоких концентрациях выявляют хлороформ - канцероген группы 2Б, по классификации МАИР.
Галоформные соединения поступают в организм с водой не только энте-рально. Некоторые вещества проникают через неповрежденную кожу во время контакта с водой, в частности при плавании в бассейне. Во время приема ванны или душа галоформные соединения попадают в воздух. Аналогичный процесс происходит в процессе кипячения воды, белья, приготовления пищи.
С учетом чрезвычайной опасности для здоровья человека галоформных соединений разработан комплекс мероприятий по снижению их уровней в воде. Он предусматривает:
Охрану источника водоснабжения от загрязнения сточными водами, которые содержат предшественники галоформных соединений;
Снижение эвтрификации поверхностных водоемов;
Отказ от перехлорирования (первичного хлорирования) или его замену ультрафиолетовым облучением или добавление меди сульфата;
Оптимизацию коагуляции для снижения цветности воды, то есть удаление гуминовых веществ (предшественников галоформных соединений);
Использование дезинфектантов, имеющих меньшую способность к образованию галоформных соединений, в частности хлора диоксида, хлораминов;
Использование хлорирования с преаммонизацией;
Аэрацию воды или использование гранулированного активированного угля в качестве наиболее эффективного способа удаления галоформных соединений из воды.
Кардинальным решением проблемы является замена хлорирования озонированием и обеззараживанием воды УФ-лучами.
Озонирование воды и его преимущества перед хлорированием. Озонирование является одним из перспективных методов обработки воды с целью ее обеззараживания и улучшения органолептических свойств. Сегодня почти 1000 водопроводных станций в Европе, преимущественно во Франции, Германии и Швейцарии, используют озонирование в технологической схеме обработки воды. В последнее время озонирование начали широко внедрять в США и Японии. В Украине озонирование используют на Днепровской водопроводной
Рис. 25. Технологическая схема озонаторной установки:
1 - воздухоприемник; 2 - воздушный фильтр; 3 - предупредительный клапан; 4 - пять приточных вентиляторов; 5 - воздушный вантуз; 6 - два охлаждаемых сушителя; 7 - четыре адсорбционные сушки; 8 - активированный глинозем; 9 - охлаждение нагревателей вентилятора; 10 - пятьдесят генераторов озона (изображено 2); 11 - сухой воздух; 12 - впуск охлаждающей воды; 13 - выпуск охлаждающей воды; 14 - озонированный воздух; 15 - три резервуара для диффузии озона; 16 - уровень воды
Станции Киева, в странах СНГ - на водопроводных станциях Москвы (Российская Федерация) и Минска (Беларусь).
Озон (Os) - газ бледно-фиолетового цвета, обладающий специфическим запахом, сильный окислитель. Молекула его весьма неустойчива, легко распадается (диссоциирует) на атом и молекулу кислорода. В промышленных условиях озоно-воздушную смесь получают в озонаторе с помощью "медленного" электрического разряда при напряжении 8000-10 000 В.
Принципиальная схема озонаторной установки приведена на рис. 25. Компрессор забирает воздух, очищает от пыли, охлаждает, сушит на адсорберах с силикагелем или активным алюминия оксидом (которые регенерируют продуванием горячим воздухом). Далее воздух проходит через озонатор, где образуется озон, который через распределительную систему подается в воду контактного резервуара. Доза озона, необходимая для обеззараживания, для большинства типов воды составляет 0,5-6,0 мг/л. Чаще всего для подземных водоисточников дозу озона принимают в пределах 0,75-1,0 мг/л, для поверхностных вод - 1-3 мг/л. Иногда для обесцвечивания и улучшения органо-лептических свойств воды необходимы высокие дозы. Продолжительность контакта озона с водой должна быть не менее 4 мин1. Косвенным показателем
*В соответствии с ГОСТом 2874-82 продолжительность обеззараживания воды с помощью озона составляла не менее 12 мин. Такая же продолжительность регламентируется и утвержденным МЗ России СанПиНом 2.1.4.559-96 "Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества". В соответствии с СанПиН "Вода питьевая. Гигиенические требования к качеству воды централизованного хозяйственно-питьевого водоснабжения", утвержденным МЗ Украины, продолжительность обработки озоном должна быть не менее 4 мин.*
Эффективности озонирования является наличие остаточных количеств озона на уровне 0,1-0,3 мг/л после камеры смешения.
Озон в воде распадается, образуя атомарный кислород: 03 -> 02 + О". Доказано, что механизм распада озона в воде сложен. При этом происходит ряд промежуточных реакций с образованием свободных радикалов (например, НО*), которые также являются окислителями. Более сильное окислительное и бактерицидное действие озона по сравнению с хлором объясняется тем, что его окислительный потенциал больше, чем у хлора.
С гигиенической точки зрения, озонирование является одним из наилучших методов обеззараживания воды. Вследствие озонирования достигается надежный обеззараживающий эффект, разрушаются органические примеси, а органолептические свойства воды не только не ухудшаются, как при хлорировании или кипячении, но и улучшаются: уменьшается цветность, исчезают лишние привкус и запах, вода приобретает голубой оттенок. Избыток озона быстро разлагается, образуя кислород.
Озонирование воды имеет следующие определенные преимущества перед хлорированием:
1) озон является одним из самых сильных окислителей, его окислительно-восстановительный потенциал выше, чем у хлора и даже хлора диоксида;
2) при озонировании в воду не вносится ничего постороннего и не происходит сколько-нибудь заметных изменений минерального состава воды и pH;
3) избыток озона через несколько минут превращается в кислород, и поэтому не влияет на организм и не ухудшает органолептические свойства воды;
4) озон, вступая во взаимодействие с соединениями, содержащимися в воде, не вызывает появления неприятных привкусов и запахов;
5) озон обесцвечивает и дезодорирует воду, содержащую органические вещества природного и промышленного происхождения, придающие ей запах, привкус и окраску;
6) по сравнению с хлором озон эффективнее обеззараживает воду от споровых форм и вирусов;
7) процесс озонирования в меньшей степени подвержен влиянию переменных факторов (pH, температуры и т. п.), что облегчает технологическую эксплуатацию водоочистных сооружений, а контроль за эффективностью не сложней, чем при хлорировании воды;
8) озонирование воды обеспечивает бесперебойность процесса обработки воды, отпадает необходимость перевозки и хранения небезопасного хлора;
9) при озонировании образуется значительно меньше новых токсических веществ, чем при хлорировании. Преимущественно это альдегиды (например, формальдегид) и кетоны, которые образуются в сравнительно небольших количествах;
10) озонирование воды дает возможность комплексной обработки воды, при которой может одновременно достигаться обеззараживание и улучшение органолептических свойств (цветность, запах и привкус).
Обеззараживание воды ионами серебра. Вода, обработанная серебром в дозе 0,1 мг/л, сохраняет высокие санитарно-гигиенические показатели в течение года. Вводить серебро можно непосредственно, путем обеспечения контакта воды с поверхностью самого металла, а также растворяя соли серебра в воде электролитическим способом. Л.А. Кульский разработал ионаторы ЛК-27, ЛК-28, в которых предусматривается анодное растворение серебра электрическим постоянным током.
Механизм действия химических дезинфектантов на микроорганизмы. Начальной стадией действия любого дезинфектанта на бактериальную клетку является его сорбция на клеточной поверхности (О.С. Савлук, 1998). После диффузии дезинфектантов сквозь клеточную стенку мишенями их действия становятся цитоплазматическая мембрана, нуклеоид, цитоплазма, рибосомы, мезосомы. Следующий этап - деградация макромолекулярных, в том числе белковых, структур бактериальной клетки в результате инактивации высокореактивноспособных функциональных групп (сульфгидрильных, аминных, фе-нольных, индольных, тиоэтиловых, фосфатных, кетогрупп, эндоциклических атомов азота и пр.). Наиболее чувствительными являются ферменты, содержащие SH-группы, т. е. тиоловые ферменты. Среди них наиболее сильно угнетаются дегидрогеназы, которые обеспечивают дыхание бактерий и локализованы преимущественно в мезосомах.
Среди органелл бактериальной клетки одной из наиболее повреждаемых химическими дезинфектантами является цитоплазматическая мембрана. Это обусловлено ее легкой доступностью для окислителя (сравнительно с другими органеллами) и наличием большого количества активных групп (в том числе сульфгидрильных), которые легко инактивируются. Поэтому для повреждения цитоплазматической мембраны необходимы сравнительно незначительные количества дезинфектантов. Ввиду важности функций цитоплазматической мембраны для жизнедеятельности бактериальной клетки, ее повреждение является чрезвычайно опасным.
Нуклеоид, основную часть которого представляет молекула ДНК, несмотря на наличие реактивноспособных групп, которые потенциально способны взаимодействовать с дезинфектантами, малодоступен для их молекул и ионов. Это вызвано, во-первых, трудностями транспорта дезинфектанта из водного раствора в нуклеоид через внешнюю и цитоплазматическую мембраны бактериальной клетки, а отсюда -- с непродуктивными потерями обеззараживающих агентов. Во-вторых, наличие первичной гидратной оболочки на поверхности ДНК становится препятствием для некоторых дезинфектантов. В частности, эта гидратная оболочка непроницаема для катионов.
Значительное количество дезинфектанта необходимо для инактивации рибосом и полисом, которые содержат рРНК, что обусловлено их высокой концентрацией в бактериальной клетке (по сравнению с ДНК).
Химические дезинфектанты должны иметь максимально широкий спектр бактерицидного действия и минимальную токсичность для организма. С учетом механизма взаимодействия с бактериальными клетками химические дезинфектанты разделены на две группы:
1. Вещества, которые поражают клеточные структуры за счет химико-физического воздействия, т. е. вещества полярной структуры, которые содержат липофильные и гидрофильные группы (спирты, фенолы, крезолы, детергенты, полипептидные антибиотики). Растворяют фрагменты клеточных структур - мембран, нарушая их целость и соответственно функции. Обладая широким спектром бактерицидного действия благодаря сходству строения клеточных мембран у разнообразных прокариотов, этот класс дезинфектантов эффективен лишь в высоких концентрациях - от 1 до 10 М.
2. Вещества, поражающие клеточные структуры за счет химического взаимодействия. Их можно разделить на 2 подкласса: 1) вещества, которые только тормозят рост бактерий; 2) вещества, вызывающие их гибель. Грань между ними достаточно условна и в большой степени определяется концентрацией. К дезинфектантам, которые вызывают гибель клеток, принадлежат почти все тяжелые металлы, образующие с сульфгидрильными группами тяжело диссоциируемые комплексы, а также циан-анионы, которые образуют тяжело диссоциируемые комплексы с железом, чем блокируют функцию терминального дыхательного фермента цитохромоксидазы. Дезинфектанты, которые тормозят рост бактерий, при взаимодействии с функциональными группами клеточных соединений или приводят к их превращению (обратимому в определенных условиях) в другие группы, или ингибируют их вследствие структурного подобия дезинфектантов с нормальными клеточными метаболитами.
Эффективность действия химических дезинфектантов зависит и от возможностей их транспорта через клеточные структуры к мишени в клетке. У грациликутных (грамотрицательных) и фирмакутных (грамположительных) бактерий оболочки имеют разное строение, причем основное отличие состоит в том, что грациликутные бактерии имеют дополнительную внешнюю прослойку, состоящую из фосфолипидов, липопротеинов и белков. И двух-, и трехслойная структуры оболочки обеспечивают высокую селективность проникновения извне в клетку чужеродных веществ.
Кроме транспортных ограничений, на эффективность химических дезинфектантов может влиять электролитный состав обеззараживаемой воды. Например, при использовании для дезинфекции катионов тяжелых металлов наличие некоторых анионов (С1~, Вг", I", SO^~, PO J" и пр.) и щелочная среда, может привести к образованию тяжелорастворимых плохо диссоциируемых соединений.
Взаимодействие дезинфектантов с метаболитами клетки и химическими соединениями, которые содержатся в ней, также может привести к изменению физико-химических свойств дезинфектанта. Так, по данным Л.А. Куль-ского (1988), внутриклеточная жидкость содержит почти 3 мг-экв/л анионов, до 100 мг-экв/л HPOj" и почти 20 мг-экв/л SOj", чего вполне достаточно для превращения многих дезинфектантов, например катионов тяжелых металлов, в малодиссоциированные соединения.
Механизм бактерицидного действия позволяет объяснить синергические эффекты, которые наблюдаются экспериментально при обеззараживании воды комбинациями химических дезинфектантов или путем физического влияния и действия химического дезинфектанта. С позиции рассмотренного механизма, действием одного из комбинации дезинфектантов нейтрализуется система "жертвенной защиты" бактериальной клетки, после чего другой дезинфектант получает практически беспрепятственный доступ к основным мишеням и, взаимодействуя с ними, инактивирует клетку.
Так, оптимальными бактерицидными свойствами должны обладать комбинации химических дезинфектантов, в которых один способен необратимо связывать сульфгидрильные группы белков оболочки, а другой, имеющий высокоселективные транспортные свойства, быстро диффундирует в цитоплазму клетки и, взаимодействуя с ДНК и РНК, инактивирует бактериальную клетку.Такими высокоэффективными комбинациями дезинфектантов являются системы С12: Н202, С12: 03, С12: Ag+, I2: Ag+ и т. п. При сочетании физического влияния и действия химического дезинфектанта в результате физического воздействия на оболочку бактериальной клетки происходит дезорганизация или частичное разрушение ее структуры. Это способствует более легкой транспортировке химического дезинфектан-та к мишеням клетки и ее дальнейшей инактивации. Применение комбинаций дезинфектантов очень эффективно в отношении инактивации бактериальных клеток-мутантов, которые находятся в клеточных популяциях в количестве ю-4-ю-".
Рассмотренный механизм бактерицидного действия химических дезинфектантов позволяет объяснить закономерности инактивации вирусов и бактериофагов. В частности, повышенная резистентность к химическим дезинфектан-там бактериофагов по сравнению с бактериальными клетками объясняется их пребыванием в цитоплазме бактерии и таким образом низкой доступностью для большинства химических дезинфектантов. Инактивация химическими де-зинфектантами вирусов и бактериофагов вне бактериальной клетки, возможно, осуществляется благодаря денатурации белковых оболочек вируса и взаимодействия с его ферментными системами, расположенными под белковыми оболочками.
Обеззараживание воды ультрафиолетовым (УФ) облучением. Обеззараживание воды УФ-лучами относится к физическим (безреагентным) методам. Безреагентные методы имеют ряд преимуществ, при их применении не изменяется состав и свойства воды, не появляются неприятные привкусы и запахи, отпадает необходимость в транспортировке и хранении реагентов.
Бактерицидное действие оказывают участок УФ-части оптического спектра в диапазоне волн от 200 до 295 нм. Максимум бактерицидного действия приходится на 260 нм. Такие лучи проникают через 25-сантиметровый слой прозрачной и бесцветной воды. Обеззараживается вода УФ-лучами достаточно быстро. После 1-2 мин облучения гибнут вегетативные формы патогенных микроорганизмов. Мутность и особенно цветность, окраска и соли железа, снижая проницаемость воды для бактерицидных УФ-лучей, замедляют этот процесс. То есть предпосылкой надежного обеззараживания воды УФ-лучами является предварительное ее осветление и обесцвечивание.
Обеззараживают УФ-облучением с помощью бактерицидных ламп преимущественно воды подземных водоисточников, коли-индекс которых не более 1000 КОЕ/л, содержание железа - не более 0,3 мг/л. Бактерицидные установки оборудуют на всасывающих и напорных линиях насосов II подъема в
Рис. 26. Установка для обеззараживания воды УФ-лучами (OB AKX-1):
А - разрез; б - схема движения воды по камере; 1 - смотровое окно; 2 - корпус; 3 - перегородки;
4 - подача воды; 5 - ртутно-кварцевая лампа ПРК-7; 6 - кварцевый чехол отдельных зданиях или помещениях. Если продуктивность водопроводной станции до 30 м3/ч, применяют установки с непогружным источником облучения в виде аргонно-ртутных ламп низкого давления. Если продуктивность станции составляет 30-150 м3/ч, то применяют установки с погружными ртут-но-кварцевыми лампами высокого давления (рис. 26).
При использовании аргонно-ртутных ламп низкого давления в воде не образуются токсические побочные продукты, тогда как под действием ртутно-кварцевых ламп высокого давления химический состав воды может изменяться за счет фотохимических превращений растворенных в воде веществ.
Обеззараживающий эффект бактерицидных УФ-лучей обусловлен преимущественно фотохимическими реакциями, вследствие чего возникают необратимые повреждения ДНК бактериальной клетки. Кроме ДНК, УФ-лучи повреждают и другие структурные части клетки, в частности рРНК, клеточные мембраны. Выход бактерицидной энергии составляет 11% при оптимальной длине большей части излучаемых волн.
Таким образом, бактерицидные лучи не денатурируют воду и не изменяют ее органолептических свойств, а также имеют более широкий спектр абиотического действия - они губительно влияют на споры, вирусы и яйца гельминтов, устойчивые к хлору. В то же время использование этого метода обеззараживания воды усложняет оперативный контроль эффективности, так как результаты определения микробного числа и коли-индекса воды можно получить только через 24 ч инкубации посевов, а экспрессного метода, который подобен определению остаточного свободного или связанного хлора или остаточного озона, в данном случае не существует.
Обеззараживание воды ультразвуком. Бактерицидное действие ультразвука объясняется главным образом механическим разрушением бактерий в ультразвуковом поле. Данные электронной микроскопии свидетельствуют о разрушении клеточной оболочки бактерий. Бактерицидный эффект ультразвука не зависит от мутности (в пределах до 50 мг/л) и цветности воды. Он распространяется как на вегетативные, так и на споровые формы микроорганизмов и зависит лишь от интенсивности колебаний.
Ультразвуковые колебания, которые могут быть использованы для обеззараживания воды, получают пьезоэлектрическим или магнитострикционным путем. Чтобы получить воду, отвечающую требованиям ГОСТа 2874-82 "Вода питьевая. Гигиенические требования и контроль за качеством", интенсивность ультразвука должна составлять около 2 Вт/см2, частота колебаний - 48 кГц в 1 с. Ультразвук частотой 20-30 кГц уничтожает бактерии за 2-5 с.
Термическое обеззараживание воды. Метод используют для обеззараживания небольшого количества воды в санаториях, больницах, на пароходах, поездах и пр. Полное обеззараживание воды и гибель патогенных бактерий достигается через 5-10 мин кипячения воды. Для этого типа обеззараживания используют специальные типы кипятильников.
Обеззараживание рентгеновским излучением. Метод предусматривает облучение воды коротковолновым рентгеновским излучением длиной волны 60-100 нм. Коротковолновое излучение глубоко проникает в бактериальные клетки, обусловливает их значительные изменения и ионизацию. Метод изучен недостаточно.
Обеззараживание вакуумированием. Метод предусматривает инактивацию бактерий и вирусов при пониженном давлении. Полный бактерицидный эффект достигается в течение 15-20 мин. Оптимальный режим обработки - при температуре 20-60 °С и давлении 2,2-13,3 кПа.
Другие физические методы обеззараживания, такие как обработка у-облу-чением, высоковольтными разрядами, электрическими разрядами малой мощности, переменным электрическим током, используют ограничено вследствие их высокой энергоемкости, сложности аппаратуры, а также из-за их недостаточной изученности и отсутствия информации о возможности образования вредных побочных соединений. Большинство из них сегодня находятся на стадии научных разработок.
Обеззараживание воды в полевых условиях. Система водоснабжения в полевых условиях должна гарантировать получение качественной питьевой воды, не содержащей возбудителей инфекционных болезней. Из технических средств, пригодных для улучшения качества воды в полевых условиях, особого внимания заслуживают тканево-угольные фильтры (ТУФ): портативные, транспортабельные, простые и высокопродуктивные.
ТУФ конструкции М.Н. Клюканова предназначены для временного использования (водоснабжения в полевых условиях, сельской местности, на
новостройках, во время экспедиций). Очищают и обеззараживают воду по методике М.Н. Клюканова путем одновременной коагуляции и дезинфекции повышенными дозами хлора (суперхлорирование) с дальнейшей фильтрацией через ТУФ (рис. 27). На тканевом фильтрующем слое задерживаются взвешенные частиц, то есть достигается осветление и обесцвечивание воды, а на угольном фильтрующем слое осуществляется дехлорирование.
Для коагуляции используют алюминия сульфат - A12(S04)3 в количестве 100- 200 мг/л. Доза активного хлора для обеззараживания воды (суперхлорирование) составляет не менее 50 мг/л. В воду одновременно вносят коагулянт и хлорную известь или ДТСГК (двутретиосновную соль гипо-
Хлорита кальция) в дозах 150 и 50 мг/л соответственно. В этом случае на коагуляцию не влияет щелочность воды:
А) с хлорной известью -
A12(S04)3 + 6СаОС12 + 6Н20 -> -> 2А1(ОН)3 + 3CaS04 + ЗСаС12 + 6HOCI;
Б) с ДТСГК -
A12(S04)3 + ЗСа(ОС1)2 2Са(ОН)2 + 2Н20 -> ->2А1(ОН)3 + 3CaS04 + 2Са(ОС1)2 + 2НОС1.
Обычно коагуляция происходит по реакции алюминия сульфата с гидрокарбонатами воды, которых должно быть не менее 2 мг-экв/л. В других случаях воду необходимо подщелачивать.
Через 15 мин после обработки приведенными выше реактивами отстоянную воду фильтруют через ТУФ. В очищенной воде определяют остаточный хлор и органолептические свойства.
Водопроводная сеть и сооружения на ней. Водопроводная сеть (распределительная система водопровода) представляет собой подземную систему труб, по которым вода под давлением (не менее 2,5-4 атм при пятиэтажной застройке), создаваемым насосной станцией II подъема, подается в населенный пункт и разводится на его территории. Она состоит из основных водоводов, по которым вода с водопроводной станции поступает в населенный пункт, и разветвленной сети труб, по которым вода подводится к водонапорным резервуарам, внешним водозаборным сооружениям (уличным колонкам, пожарным гидрантам), жилым и общественным зданиям. При этом основной водовод разветвляется на несколько магистральных, которые в свою очередь разветвляются на уличные, дворовые и домовые. Последние соединяются с системой труб внутреннего водопровода жилых и общественных зданий.
Рис. 28. Схема водопроводной сети: А - тупиковая схема; Б - кольцевая схема; а - насосная станция; б - водопровод; в - водонапорная башня; г - заселенные кварталы; д - разводящая сеть
По конфигурации водопроводная сеть может быть: 1) кольцевой; 2) тупиковой; 3) смешанной (рис. 28). Тупиковая сеть состоит из отдельных глухих линий, в которые вода поступает с одной стороны. При повреждении такой сети на каком-либо участке прекращается подача воды всем потребителям, которые подключены к линии, расположенной за точкой повреждения в направлении движения воды. В тупиковых концах распределительной сети вода может застаиваться, может появляться осадок, который служит благоприятной средой для размножения микроорганизмов. Тупиковую водопроводную сеть как исключение оборудуют на небольших поселковых и сельских водопроводах.
Наилучшей с гигиенической точки зрения является замкнутая водопроводная сеть, которая состоит из системы смежных замкнутых контуров, или колец. Повреждение на каком-либо участке не приводит к прекращению подачи воды, так как она может поступать по другим линиям.
Распределительная система водопровода должна обеспечить бесперебойную подачу воды во все точки ее потребления и предотвратить загрязнение воды на всем пути ее поступления от главных водопроводных сооружений до потребителей. Для этого водопроводная сеть должна быть водонепроницаемой. Загрязнение воды в водопроводной сети при централизованном водоснабжении вызывают: нарушение герметичности водопроводных труб, значительное снижение давления в водопроводной сети, что приводит к подсасыванию загрязнения в негерметичных участках, и наличие источника загрязнения вблизи участка нарушения герметичности водопроводных труб. Объединять сети хозяйственно-питьевого водопровода с сетями, подающими непитьевую воду (технический водопровод), недопустимо.
Водопроводные трубы изготавливают из чугуна, стали, железобетона, пластмасс и т. п. Трубы из полимерных материалов, а также внутренние антикоррозийные покрытия используют только после их гигиенической оценки и получения разрешения Министерства здравоохранения. Стальные трубы применяют на участках с внутренним давлением свыше 1,5 МПа, при пересечении с железнодорожными путями, автомобильными дорогами, поверхностными водоемами (реки), в местах пересечения хозяйственно-питьевого водопровода с канализацией. Они нуждаются в защите наружной и внутренней поверхностей от коррозии. Диаметр труб хозяйственно-питьевого водопровода в городских населенных пунктах должен быть не менее 100 мм, в сельских - более 75 мм. Герметичного соединения отдельных отрезков труб длиной 5-10 м достигают с помощью фланцев, раструбов или муфт (рис. 29). Фланцевые соединения применяют лишь при открытом (на поверхности земли) прокладывании труб, где они доступны для внешнего осмотра и проверки герметичности.
Прокладыванию водопроводных линий хозяйственно-питьевого водоснабжения должна предшествовать санитарная оценка территории не менее чем на 40 м в обе стороны при расположении водопровода на незастроенной территории и на 10-15 м - на застроенной. Почва, по которой будет проложена трасса водопровода, должна быть незагрязненной. Трассу не следует прокладывать по болотам, свалкам, кладбищам, скотомогильникам, то есть там, где почва загрязнена. Вдоль водопроводов необходимо организовать санитарно-за-щитную полосу (см. с. 129, 130).
Водопроводные трубы должны быть проложены на 0,5 м ниже уровня распространения в почве нулевой температуры (уровня замерзания почвы). При этом в зависимости от климатического района глубина заложения труб колеблется от 3,5 до 1,5 м. В южных регионах для предотвращения перегревания воды в летнее время глубина прокладывания водопроводных труб должна быть такой, чтобы слой почвы над трубой был толщиной не менее 0,5 м.
Водопроводные линии нужно прокладывать на 0,5 м выше канализационных. Если водопроводные трубы прокладываются на одном уровне с параллельно проложенными канализационными линиями, расстояние между ними должно составлять не менее 1,5 м при диаметре водопроводных труб до 200 мм и не менее 3 м - при диаметре свыше 200 мм. При этом необходимо использовать металлические трубы. Металлические водопроводные трубы применяют также в местах их пересечения с канализационными линиями. При этом водопроводные трубы следует прокладывать на 0,5 м выше канализационных. Как исключение в местах пересечения водопроводные трубы можно располагать ниже канализационных. При этом разрешают использовать только стальные водопроводные трубы, дополнительно защитив их специальным металлическим кожухом длиной не менее 5 м в обе стороны от пересечения в глинистых грунтах и не менее 10 м - в грунтах с высокой фильтрационной способностью (например, песчаных). Канализационные трубы на указанном участке должны быть чугунными.
На водоводах и линиях водопроводной сети устанавливают: поворотные затворы (засовы) для выделения ремонтных участков; вантузы - для выпуска воздуха во время работы трубопроводов; клапаны - для выпуска и впуска воздуха при освобождении трубопроводов от воды на время ремонта и последующего заполнения; выпуски - для сбрасывания воды при опорожнении трубопроводов; регуляторы давления, клапаны для защиты от гидравлических ударов, если неожиданно потребуется отключить или включить насосы и т. п. Длина ремонтных участков при прокладывании водопроводов в одну линию не должна превышать 3 км, в две линии и более - 5 км.
Запорную, регулировочную и охранную арматуру устанавливают в смотровых водопроводных колодцах. Смотровые колодцы также оборудуют во всех местах стыков основных, магистральных и уличных водопроводов. Колодцы - это размещенные под землей водонепроницаемые железобетонные шахты. Для спуска в смотровой колодец предусмотрен люк с герметично закрытой крышкой, которую утепляют в холодный период года; в стену вмонтированы чугунные или стальные скобы. Опасность загрязнения воды в водопроводной сети через смотровые колодцы возникает при заполнении шахты водой. Это может произойти в результате поступления воды через негерметичные стенки и дно, ливневых вод через негерметично закрытую крышку или воды из водопроводной сети через негерметичные стыки труб и арматуры. Во время снижения давления в сети вода, которая собралась в смотровом колодце, может подсасываться в трубы.
Водонапорные (запасные) резервуары предназначены для создания запаса воды, который компенсирует возможное несоответствие между подачей воды и ее потреблением в отдельные часы суток. Наполняют резервуары преимущественно ночью, а днем в часы интенсивного водопользования вода из них поступает в сеть, нормализуя давление.
Устанавливают водонапорные резервуары в наиболее высокой точке рельефа на башнях, возвышающихся над наиболее высокими зданиями населенного пункта (рис. 30). Территорию вокруг водонапорных башен ограждают. Резервуары должны быть водонепроницаемы, из железа или железобетона. Для очистки, ремонта и обеззараживания внутренней поверхности резервуара
Рис. 30. Водонапорная башня: а - внешний вид; б - разрез: I - подающе-разводящая труба; 2 - переливная труба
Предусмотрены люки с плотно закрытыми и запломбированными крышками. Для воздухообмена резервуаров оборудуют вентиляционные отверстия, закрытые сетками и защищенные от атмосферных осадков. На трубах, подающих и отводящих воду, устанавливают краны для отбора проб воды с целью контроля ее качества до и после резервуара. Водонапорные резервуары нуждаются в периодической (1-2 раза в год) дезинфекции.
На больших водопроводах запасные резервуары - резервуары чистой воды - оборудуют под землей. Из них воду подают в водопроводную сеть насосными станциями III подъема.
Водоразборные колонки. Население берет воду из водораспределительной системы или через домовые вводы и краны внутридомовой водопроводной сети, или через наружные водоразборные сооружения - колонки.
Уличные водоразборные колонки являются наиболее уязвимыми элементами водопровода. Известно немало случаев эпидемических вспышек инфекционных болезней, которые получили название эпидемии "одной колонки"
Существуют разные конструкции колонок, но наиболее распространенные - системы Черкунова и московского типа. Устанавливают их в районах застройки без ввода труб централизованного хозяйственно-питьевого водопровода в сооружения. При этом радиус обслуживания колонки должен быть не более 100 м. В последнее время в городах при централизованном водоснабжении с забором воды из поверхностных водоемов колонки широко применяют для организации бюветного артезианского водоснабжения1.
Водоразборная колонка системы Черкунова (рис. 31) состоит из наземной и подземной частей. Подземная часть (смотровой колодец) имеет вид шахты с водонепроницаемыми железобетонными стенками и дном. Там размещены эжектор (его устанавливают на пути движения воды из водопроводной магистрали во внутреннюю водяную трубку колонки) и сливной бачок с воздушной трубкой. В железобетонном перекрытии шахты расположен герметично закрытый люк. Наземная часть колонки имеет выводную трубку и ручку, которая штангой соединена с клапаном, расположенным перед эжектором на выходе воды из водопроводной магистрали. Вокруг колонки в радиусе 1,5-2 м оборудуют отмостку с наклоном от колонки, под выводной трубой - лоток для отведения воды, пролившейся во время пользования.
При нажатии ручки открывается клапан, и вода из водопроводной магистрали под давлением поднимается по водяной трубе и выливается через выводную трубу колонки. Когда ручку отпускают, клапан закрывается. Поскольку вода, оставшаяся в водяной трубе, в холодный период года замерзает и разрывает трубу, то предусмотрен ее слив в металлический бачок на дне смотрового колодца. При этом воздух из бачка через воздушную трубку поступает в шахту. При повторном нажатии ручки и открывании клапана вода, выходя под давлением через суженное отверстие водопроводной магистрали в водяную трубу, приводит в действие эжектор. Эффект эжекции (подсасывания), который возникает в первые секунды после открытия клапана и длится недолго, подсасывает воду из бачка в водяную трубку. Бачок через воздушную трубу заполняется воздухом из шахты. Таким образом, первые порции воды, поступающие из колонки сразу после нажатия ручки, являются смесью воды из водопроводной сети и сливного бачка. Вследствие подсасывания воды из бачка давление в эжекторе выравнивается, эффект эжекции исчезает, после чего к потребителю поступает вода исключительно из водопроводной сети. Когда ручку отпускают, бачок снова наполняется водой из водяной трубки колонки.
Реальная угроза загрязнения воды в колонке может возникнуть в том случае, если шахта колонки заполнится водой. Пути поступления воды в шахту могут быть различными. Так, атмосферные осадки и поверхностный сток
*Бюветное водоснабжение осуществляется за счет локального водопровода. Его элементами являются: 1) подземный межпластовый (желательно, артезианский) источник I класса по ГОСТу 2761-84; 2) артезианская скважина; 3) подземная насосная станция с погружным центробежным насосом; 4) напорный водовод; 5) бювет с водоразборными колонками (преимущественно московского типа). Бюветное артезианское водоснабжение широко распространено в Киеве, где централизованное водоснабжение осуществляется за счет Днепровского и Деснянского речных и артезианского водопроводов.*
Рис. 31. Водоразборная колонка системы Черкунова: 1 - деталь эжектора и бачка; 2 - инжектор; 3 - муфта; 4 - суженный конец водопроводной трубы; 5 - противовес; 6 - лоток; 7 - штукатурка; 8 - настил из досок; 9 - воздушная трубка; 10 - водяная труба; 11 -эжектор; 12 - скобы; 13 - штанга; 14 - песок; 15 - клапан (38 мм); 16 - запорный кран; 17 - бачок
Могут проникать в смотровой колодец через неплотное перекрытие или негерметичный люк. При нарушении целости железобетонных стенок и дна шахты вода может поступить из почвы (почвенная влага, которая образуется при фильтрации атмосферных и талых вод), особенно при высоком уровне стояния грунтовых вод. Шахта может быть залита водой, поступившей из водопроводной сети. Это происходит при снижении давления в сети ниже 1 атм. При этом
Зрачности и повышение цветности ухудшают органолептические свойства колодезной и родниковой воды, ограничивают ее использование, а иногда свидетельствуют о загрязнении воды в результате погрешностей в оборудовании водозаборных сооружений (колодцев или каптажей родников), неправильного их размещения относительно потенциальных источников загрязнения, или неправильной эксплуатации. Иногда причиной снижения прозрачности и повышения цветности колодезной и родниковой воды может быть высокая концентрация солей железа (свыше 1 мг/л).
В колодезной воде, которая является эпидемически безопасной, индекс БГКП обычно не превышает 10 (коли-титр не менее 100), микробное число - не более 400 в 1 см3. При таких санитарно-микробиологических показателях в воде не определяют возбудителей кишечных инфекций, имеющих водный фактор передачи.
Содержание нитратов в колодезной и родниковой воде не должно превышать 45 мг/л, в перерасчете на азот нитратов - 10 мг/л. Превышение указанной концентрации может обусловить водно-нитратную метгемоглобинемию (острый токсический цианоз) у младенцев, находящихся на искусственном вскармливании, вследствие использования воды с высоким содержанием нитратов для приготовления питательных смесей. Незначительное повышение уровня метгемоглобина в крови без угрожающих признаков гипоксии может наблюдаться и у детей в возрасте от 1 до 6 лет, а также у людей пожилого возраста.
Увеличение содержания аммонийных солей, нитритов и нитратов в колодезной и родниковой воде может свидетельствовать о загрязнении почвы, через которую фильтруется питающая источник вода, а также о том, что одновременно с этими веществами могли попасть патогенные микроорганизмы. При свежем загрязнении в воде увеличивается содержание аммонийных солей. Наличие нитратов в воде при условии отсутствия аммиака и нитритов свидетельствует о сравнительно давнем поступлении в воду азотсодержащих веществ. При систематическом загрязнении в воде выявляют как аммонийные соли, так и нитриты и нитраты. К увеличению содержания нитратов в грунтовых водах также приводит интенсивное использование в сельском хозяйстве азотных удобрений. Повышение перманганатной окисляемости грунтовой воды свыше 4 мг/л свидетельствует о возможном загрязнении легкоокисляющимися веществами минерального и органического происхождения.
Одним из показателей загрязнения местных водоисточников водоснабжения являются хлориды. В то же время высокие концентрации (свыше 30-50 мг/л) хлоридов в воде могут быть вызваны их вымыванием из солончаковых почв. При таких условиях в 1 л воды могут содержаться сотни и тысячи миллиграммов хлоридов. Вода с содержанием хлоридов свыше 350 мг/л имеет солоноватый вкус и отрицательно влияет на организм. Для правильной оценки происхождения хлоридов следует учесть их наличие в воде соседних однотипных водоисточников, а также другие показатели загрязнения.
В отдельных случаях каждый из этих показателей может иметь и другую природу. Например, органические вещества могут быть растительного происхождения. Поэтому воду из местного источника можно считать загрязненной только при следующих условиях: 1) повышен не один, а несколько санитарно-химических показателей загрязнения; 2) одновременно повышены санитарно-микробиологические показатели эпидемической безопасности - микробное число и коли-индекс; 3) возможность загрязнения подтверждается данными санитарного обследования колодца или каптажа родника.
Гигиенические требования к размещению и устройству шахтных колодцев. Шахтный колодец - это сооружение, при помощи которого население набирает грунтовую воду и поднимает ее на поверхность. В условиях местного водоснабжения одновременно выполняет функции водозаборного, водоподъемного и водоразборного сооружений.
При выборе места размещения колодца, кроме гидрогеологических условий, необходимо учитывать санитарные условия местности и удобство пользования колодцем. Расстояние от колодца до потребителя не должно превышать 100 м. Колодцы размещают по уклону местности выше всех источников загрязнения, расположенных и на поверхности, и в толще грунта. При соблюдении этих условий расстояние между колодцем и источником загрязнения (площадкой для подземной фильтрации, выгребом, компостом и пр.) должно быть не менее 30-50 м. Если потенциальный источник загрязнения расположен выше по рельефу местности, чем колодец, то расстояние между ними в случае мелкозернистой почвы должно быть не менее 80-100 м, а иногда даже 120-150 м.
Научно обосновать величину санитарного разрыва между колодцем и потенциальным источником загрязнения почвы можно по формуле Салтыкова - Белицкого, в которой учтены местные почвенные и гидрогеологические условия. Расчет основывается на том, что загрязнения, продвигаясь вместе с грунтовыми водами в направлении колодца, не должны достичь места водозабора, то есть должно быть достаточно времени для обеззараживания загрязнения. Расчет производят по формуле:
Где L - допустимое расстояние между источником загрязнения и точкой водозабора (м), к - коэффициент фильтрации1 (м/сут) определяют экспериментально либо по таблицам, п, - уровень подземных вод в районе загрязнения водоносного горизонта, определяется экспериментально нивелиром; п2 - уровень воды водоносного горизонта в точке водозабора; t - необходимое время движения воды между источником загрязнения и точкой водозабора (это время принимается равным для бактериальных загрязнений 200 сут, а для химических - 400 сут); ц - активная пористость почвы2.
*Коэффициент фильтрации - расстояние, которое проходит вода в почве, двигаясь вертикально вниз под действием силы тяжести. Зависит от механического состава почвы. Составляет для среднезернистых песков - 0,432, для мелкозернистых - 0,043, для суглинков - 0,0043 м/сут.*
*Активная пористость - это соотношение объема пор образца водовмещающей породы к общему объему образца. Зависит от механического состава грунта: для крупнозернистых песков - 0,15, для мелкозернистых - 0,35.*
Эта формула пригодна для расчетов лишь в том случае, когда водовмеща-ющей породой являются мелко- и среднезернистые пески. Если водовмещаю-щей слой представлен крупнозернистыми песками или даже гравелистыми грунтами, к найденой величине следует добавить коэффициент запаса А:
Коэффициент определяют по формуле: А = ai + а2 + а3, где а! - радиус воронки депрессии1 максимально составляет для крупнозернистых песков 300- 400 м, для среднего гравия - 500-600 м; а2 - расстояние, на которое распространяется факел загрязнения (в зависимости от мощности источника загрязнения колеблется от 10 до 100 м); а3 - величина охранной зоны, нарушающей гидравлическую связь между факелом загрязнения и периферическим концом радиуса воронки депрессии (10-15 м).
Колодец - это вертикальная шахта квадратного или круглого сечения (площадью приблизительно 1 м2), которая доходит до водоносного слоя (рис. 33). Дно оставляют открытым, а боковые стенки закрепляют водонепроницаемым материалом (бетон, железобетон, кирпич, дерево и др.). На дно колодца насыпают слой гравия толщиной 30 см. Стенки колодца должны подниматься над поверхностью земли не менее чем на 1 м. Вокруг колодца оборудуют глиняный замок и отмостку для предупреждения просачивания вдоль стенок колодца (снаружи) загрязнений, которые вымываются из поверхностных слоев почвы. Для строительства глиняного замка вокруг колодца выкапывают яму глубиной 2 м, шириной 1 м и заполняют ее жирной глиной. Для отмостки вокруг наземной части колодца поверх глиняного замка в радиусе 2 м делают подсыпку песком и заливают цементом или бетоном с уклоном для отведения в сторону от колодца атмосферных осадков и воды, разливающейся при пользовании колодцем. Для отведения ливневых вод устраивают перехватывающую канаву. В радиусе 3-5 м вокруг общественных колодцев должно быть сделано ограждение для ограничения подъезда транспорта.
Подъем воды из колодца желательно осуществлять при помощи насоса. Если это невозможно, то оборудуют коловорот с закрепленным на нем общественным ведром. Пользоваться собственным ведром недопустимо, так как с этим связана наибольшая опасность загрязнения воды в колодце. Сруб колодца плотно закрывают крышкой и над срубом и коловоротом делают навес.
Каптажем называется специальное сооружение для сбора родниковой воды (рис. 34). Место выхода воды должно быть ограждено водонепроницаемыми стенками и закрыто сверху. Чтобы в родник не попадали поверхностные стоки, устраивают отводные канавы. Вокруг стенок каптажа оборудуют замок из жирной глины и отмостку. Материалами для каптажных сооружений могут
*Воронка депрессии - зона пониженного давления, формирующаяся в водовмещающей породе при откачивании воды из колодца вследствие сопротивления, которое оказывает порода. Зависит от механического состава породы и скорости откачивания воды.*
Рис. 33. Общий вид шахтного колодца: 1 - донный трехслойный фильтр; 2 - железобетонные кольца из пористого бетона; 3 - железобетонные кольца; 4 - крышка; 5 - лазовые скобы; 6 - каменная отмостка; 7 - коловорот; 8 - глиняный замок; 9 - крышка навеса
Быть бетон, железобетон, кирпич, камень, дерево. Чтобы вода в каптаже не поднималась выше определенного уровня, на этом уровне оборудуют переливную трубу.
Санация шахтных колодцев. Санация шахтного колодца - это комплекс мероприятий по ремонту, очистке и дезинфекции колодца с целью предупреждения загрязнения воды в нем.
С профилактической целью санацию колодца проводят перед вводом его в эксплуатацию, а далее, если эпидемическая ситуация благоприятна, нет загрязнения и жалоб от населения на качество воды, - периодически раз в год после очистки и текущего ремонта. Обязательным является проведение
Рис. 34. Простой каптаж нисходящего родника: 1 - водоносный слой; 2 - водоупорный слой; 3 - гравийный фильтр; 4 - приемная камера; 5 - смотровой колодец; 6 - люк смотрового колодца с крышкой;7 - вентиляционный люк;8 - перегородка; 9 - выпуск в канализацию или ров; 10 - труба, подающая воду потребителю
Профилактической дезинфекции после капитального ремонта колодца. Профилактическая санация состоит из двух этапов: 1) очистки и ремонта; 2) дезинфекции.
Если имеются эпидемиологические основания считать колодец очагом распространения острых желудочно-кишечных инфекционных заболеваний, а также, если имеется подозрение (тем более данные) о загрязнении воды фекалиями, трупами животных, другими посторонними предметами, санацию проводят по эпидпоказаниям. Санацию по эпидпоказаниям проводят в три этапа: 1) предварительная дезинфекция; 2) очистка и ремонт; 3) заключительная дезинфекция.
Методика санации шахтных колодцев. Санацию по эпидпоказаниям начинают с дезинфекции подводной части колодца объемным способом. Для этого определяют объем воды в колодце и рассчитывают необходимое количество хлорной извести или кальция гипохлорита по формуле:
Где Р - количество хлорной извести или кальция гипохлорита (г), Е - объем воды в колодце (м3); С - заданная концентрация активного хлора в воде колодца (100-150 г/м3), достаточная для обеззараживания стенок сруба и гравийного фильтра на дне, H - содержание активного хлора в хлорной извести или в кальции гипохлорите (%); 100 - постоянный числовой коэффициент. Если вода в колодце очень холодная (+4 °С...+6 °С), количество хлорсодержащего препарата для дезинфекции колодца объемным способом увеличивают вдвое. Рассчитанное количество дезинфектанта растворяют в небольшом объеме воды в ведре до получения равномерной смеси, осветляют отстаиванием и выливают этот раствор в колодец. Воду в колодце хорошо перемешивают в течение 15-20 мин шестами или частым опусканием и подниманием ведра на тросе. Затем колодец закрывают крышкой и оставляют на 1,5-2 ч.
После предварительной дезинфекции из колодца полностью откачивают воду насосом или ведрами. Перед тем как человек спускается в колодец, проверяют, не накопился ли там С02, для чего в ведре на дно колодца опускают зажженную свечу. Если она гаснет, то работать можно только в противогазе.
Затем производят очистку дна от ила, грязи, мусора и случайных предметов. Стенки сруба очищают механическим путем от загрязнений и обрастаний и при необходимости ремонтируют. Выбранные из колодца грязь и ил помещают в яму на расстоянии не менее 20 м от колодца на глубину 0,5 м, заливают 10% раствором хлорной извести или 5% раствором кальция гипохлорита и закапывают.
Для окончательной дезинфекции наружную и внутреннюю поверхность сруба орошают из гидропульта 5% раствором хлорной извести или 3% раствором кальция гипохлорита из расчета 0,5 дм3 на 1 м2 площади. Затем ждут, пока колодец наполнится водой до обычного уровня, после чего дезинфицируют подводную его часть объемным способом из расчета 100-150 мг активного хлора на 1 л воды в колодце в течение 6-8 ч. По истечении указанного времени контакта берут пробу воды из колодца и проверяют ее на наличие остаточного хлора или делают пробу на запах. Если запах хлора отсутствует, добавляют 1/4 или 1/3 от первоначального количества препарата и оставляют еще на 3-4 ч. После этого отбирают пробу воды и направляют в лабораторию территориальной СЭС для бактериологического и физико-химического анализа. Должно быть проведено не менее 3 исследований, через 24 ч каждое.
Дезинфекцию колодца с профилактической целью начинают с определения объема воды в колодце. Затем откачивают воду, чистят и ремонтируют колодец, дезинфицируют наружную и внутреннюю части сруба методом орошения, выжидают, пока колодец наполнится водой, и дезинфицируют подводную часть объемным способом.
Обеззараживание воды в колодце с помощью дозирующих патронов. Среди мероприятий по оздоровлению местного водоснабжения важное место занимает непрерывное обеззараживание воды в колодце при помощи дозирующих патронов. Показаниями к этому являются: 1) несоответствие микробиологических показателей качества воды в колодце санитарным требованиям; 2) наличие признаков загрязнения воды по санитарно-химическим показателям (обеззараживают до выявления источника загрязнения и получения положительных результатов после санации); 3) недостаточное улучшение качества воды после дезинфекции (санации) колодца (коли-титр ниже 100, коли-индекс выше 10); 4) в очагах кишечных инфекций в населенном пункте после дезинфекции колодца вплоть до ликвидации очага. Обеззараживают воду в колодце с помощью дозирующего патрона только специалисты территориальной СЭС, обязательно контролируя при этом качество воды по санитарно-химическим и микробиологическим показателям.
Дозирующие патроны представляют собой керамические емкости цилиндрической формы вместимостью 250, 500 или 1000 см3. Изготавливают их из: шамотной глины, инфузорной земли (рис. 35). В патроны засыпают хлорную известь или кальция гипохлорит и погружают их в колодец. Количество
Рис. 35. Дозирующий патрон
Необходимых для обеззараживания воды хлорсодержащих веществ зависит от многих факторов. К ним относятся: исходное качество грунтовой воды, характер, степень загрязнения и объем воды в колодце, интенсивность и режим водоразбора, скорость поступления грунтовых вод, дебит колодца. Количество активного хлора зависит и от санитарного состояния колодца: количества придонного ила, степени загрязнения сруба и т. п. Известно, что возбудители кишечных инфекций в придонном иле находят благоприятные условия и длительное время сохраняют жизнедеятельность. Вот почему длительное обеззараживание (хлорирование) воды при помощи дозирующих патронов не может быть эффективным без предварительной очистки и дезинфекции колодца.
Количество кальция гипохлорита активностью не ниже 52%, необходимое для длительного обеззараживания воды в колодце, рассчитывают по формуле:
X, = 0,07 Х2 + 0,08 Х3+ 0,02 Х4 + 0,14 Х5,
Где X, - количество препарата, необходимое для загрузки патрона (кг), Х2 - объем воды в колодце (м3), рассчитывают как произведение площади сечения колодца на высоту водяного столба; Х3 - дебит колодца (м3/ч), определяют экспериментально; Х4 - водоразбор (м3/сут), устанавливают путем опроса населения; Х5 - хлорпоглощаемость воды (мг/л), определяют экспериментально.
Формула дана для расчета количества кальция гипохлорита, содержащего 52% активного хлора. В случае дезинфекции хлорной известью (25% активного хлора) расчетное количество препарата следует увеличить в 2 раза. При обеззараживании воды в колодце в зимнее время расчетное количество препарата также увеличивают вдвое. Если содержание активного хлора в дезинфек-танте ниже расчетного, то производят перерасчет по формуле:
Где Р - количество хлорной извести или кальция гипохлорита (кг); X! - рассчитанное по предыдущей формуле количество кальция гипохлорита (кг); Н, - содержание активного хлора в кальции гипохлорите, принятое в расчет (52%о); Н2 - фактическое содержание активного хлора в препарате - кальции гипохлорите или хлорной извести (%). Кроме того, при обеззараживании воды в колодце в зимнее время расчетное количество препарата увеличивают вдвое. Для определения дебита - количества воды (в 1 м3), которое можно получить из колодца за 1 ч, в течение определенного времени быстро откачивают
Из него воду, измеряя ее количество, и регистрируют время восстановления исходного уровня воды. Рассчитывают дебит колодца по формуле:
Где D - дебит колодца (м3/ч), V - объем откачанной воды (м3); t - суммарное время, состоящее из времени откачивания и восстановления уровня воды в колодце (мин); 60 - постоянный коэффициент.
Перед заполнением патрон предварительно выдерживают в воде в течение 3-5 ч, затем заполняют рассчитанным количеством дезинфицирующего хлор-содержащего препарата, добавляют 100-300 см3 воды и тщательно перемешивают (до образования равномерной смеси). После этого патрон закрывают керамической или резиновой пробкой, подвешивают в колодце и погружают в толщу воды приблизительно на 0,5 м ниже верхнего уровня воды (на 0,2-0,5 м от дна колодца). Благодаря пористости стенок патрона активный хлор поступает в воду.
Контроль за концентрацией активного остаточного хлора в воде колодца проводят через 6 ч после погружения дозирующего патрона. Если концентрация активного остаточного хлора в воде ниже 0,5 мг/л, необходимо погрузить дополнительный патрон и провести затем соответствующий контроль эффективности обеззараживания. Если концентрация активного остаточного хлора в воде значительно выше 0,5 мг/л, извлекают один из патронов и проводят соответствующий контроль эффективности обеззараживания. В дальнейшем контролируют концентрацию активного остаточного хлора не реже одного раза в неделю, проверяя также микробиологические показатели качества воды.
В настоящее время проблема обеззараживания воды является очень актуальной, поэтому в качестве индивидульного задания была выбрана именно эта тема. Также на выбор темы индивидуального задания повлияло ее непосредственное отношение к теме моей магистерской работы.
Обеззараживание воды – мероприятия, в ходе которых происходит уничтожение микроорганизмов и вирусов, вызывающих инфекционные заболевания.
По способу воздействия на микроорганизмы методы обеззараживания воды подразделяются на термические (кипячение); олигодинамические (обработка ионами благородных металлов); физические (обеззараживание ультрафиолетовыми лучами, ультразвуком и т. д.); химические (обработка окислителями: хлором и его соединениями, озоном, перманганатом калия и т. п.) .
Термический метод
Кипячение является исключительно бытовым методом обеззараживания, однако он не дает полной гарантии гибели бактерий или их спор. Кроме того, при кипячении происходит удаление из воды растворенных в ней газов (кислорода, углекислого газа), что снижает ее вкусовые свойства.
При кипячении происходит частичное смягчение воды из-за того, что в осадок выпадает часть солей кальция и магния, которые из растворимых гидрокарбонатных солей переходят в нерастворимые карбонатные .
Обеззараживание воды серебром
Обработка воды, в которой содержится 0,05 - 0,2 мг / дм 3 серебра, втечение 30 - 60 мин дaет возможность достичь санитарных норм. Для растворения серебра в воде используют методы контактирования воды с развитой поверхностью металла, растворением солей серебра или электролитическим растворением металлического серебра. Наибольшее распространение получил последний метод, основанный на анодном растворении серебра.
Однако серебро, как и другие тяжелые металлы, способно накапливаться в организме и вызывать заболевания (аргироз – отравление серебром). Кроме того, для бактерицидного действия серебра на бактерии требуются достаточно большие концентрации, а в допустимых количествах (около 50 мкг/л) оно способно оказывать лишь бактериостатическое действие, т.е. останавливать рост бактерий, не убивая их. А некоторые виды бактерий вообще практически не чувствительны к серебру.
Все эти свойства ограничивают применение серебра. Оно может быть уместно только в целях сохранения исходно чистой воды для длительного хранения .
Обеззараживание воды ультрафиолетовыми лучами
Данный метод основан на способности ультрафиолетового излучения с определенной длиной волны губительно действовать на ферментные системы бактерий. Ультрафиолетовые лучи уничтожают не только вегетативные, но и споровые формы бактерий, и не изменяют органолептических свойств воды. Важно отметить, что поскольку при УФ-облучении не образуются токсичные продукты, то не существует верхнего порога дозы. Увеличением дозы УФ-излучения почти всегда можно добиться желаемого уровня обеззараживания. В качестве источника излучения используются ртутные лампы, изготовленные из кварцевого песка.

Метод не требует сложного оборудования и легко может применяться в бытовых комплексах водоподготовки в частных домах.
Фактором, снижающим эффективность работы установок УФ-обез¬зараживания при длительной эксплуатации, является загрязнение кварцевых чехлов ламп отложениями органического и минерального состава. Крупные установки снабжаются автоматической системой очистки, осуществляющей промывку путем циркуляции через установку воды с добавлением пищевых кислот. В остальных случаях применяется механическая очистка.
Основным недостатком метода является полное отсутствие последействия .
Ультразвуковая обработка воды
Обеззараживание воды ультразвуком основано на способности его вызывать так называемую кавитацию – образование пустот, создающих большую разность давления, что ведет к разрыву клеточной оболочки и гибели бактериальной клетки. Бактерицидное действие ультразвука разной частоты весьма значительно и зависит от интенсивности звуковых колебаний.
В настоящее время этот способ еще не нашел достаточного применения в системах очистки воды, хотя в медицине он широко используется для дезинфекции инструментария и т.п. в так называемых ультразвуковых мойках .
Озонирование
Озонирование воды основано на свойстве озона разлагаться в воде с образованием атомарного кислорода, разрушающего ферментные системы микробных клеток и окисляющего некоторые соединения, которые придают воде неприятный запах (например, гуминовые основания). Количество озона, необходимое для обеззараживания воды, зависит от степени загрязнения воды и составляет 1–6 мг/дм 3 при контакте в 8–15 мин; количество остаточного озона должно составлять не более 0,3–0,5 мг/дм 3 , т. к. более высокая доза придает воде специфический запах и вызывает коррозию водопроводных труб.  Однако молекула озона неустойчива, поэтому его остаточные количества быстро разлагаются в воде. С гигиенической точки зрения озонирование воды – один из лучших способов обеззараживания питьевой воды. При высокой степени обеззараживания воды оно обеспечивает ее наилучшие органолептические показатели и отсутствие высокотоксичных и канцерогенных продуктов в очищенной воде.
Однако молекула озона неустойчива, поэтому его остаточные количества быстро разлагаются в воде. С гигиенической точки зрения озонирование воды – один из лучших способов обеззараживания питьевой воды. При высокой степени обеззараживания воды оно обеспечивает ее наилучшие органолептические показатели и отсутствие высокотоксичных и канцерогенных продуктов в очищенной воде.
Однако в связи с большим расходом электроэнергии, использованием сложной аппаратуры и необходимостью высококвалифицированного обслуживания, озонирование нашло применение для обеззараживания питьевой воды только при централизованном водоснабжении.
Метод озонирования воды технически сложен и наиболее дорогостоящ. Технологический процесс включает последовательные стадии очистки воздуха, его охлаждения и осушки, синтеза озона, смешения озоновоздушной смеси с обрабатываемой водой, отвода и деструкции остаточной озоновоздушной смеси, вывода ее в атмосферу. Все это требует также дополнительного вспомогательного оборудования (озонаторы, компрессоры, установки осушки воздуха, холодильные агрегаты и т. д.), объемных строительно-монтажных работ.
Озон токсичен. Предельно допустимое содержание этого газа в воздухе производственных помещений 0,1 г/м3. К тому же существует опасность взрыва озоновоздушной смеси .
Хлорирование
Наиболее распространенным методом обеззараживания воды был и остается метод хлорирования. Это объясняется высокой эффективностью, простотой используемого технологического оборудования, дешевизной применяемого реагента – жидкого или газообразного хлора – и относительной простотой обслуживания.
Очень важным и ценным качеством метода хлорирования является его последействие. Если количество хлора взято с некоторым расчетным избытком, так чтобы после прохождения очистных сооружений в воде содержалось 0,3–0,5 мг/л остаточного хлора, то не происходит вторичного роста микроорганизмов в воде.
Хлор является сильнодействующим токсическим веществом, требующим соблюдения специальных мер по обеспечению безопасности при его транспортировке, хранении и использовании; мер по предупреждению катастрофических последствий в чрезвычайных аварийных ситуациях. Поэтому ведется постоянный поиск реагентов, сочетающих положительные качества хлора и не имеющих его недостатков.
Предлагается применение диоксида хлора, который обладает рядом преимуществ, таких как: более высокое бактерицидное и дезодорирующее действие, отсутствие в продуктах обработки хлорорганических соединений, улучшение органолептических качеств воды, отсутствие необходимости перевозки жидкого хлора. Однако диоксид хлора дорог, должен производиться на месте по достаточно сложной технологии. Его применение имеет перспективу для установок относительно небольшой производительности.
Применение для обеззараживания воды хлорсодержащих реагентов (хлорной извести, гипохлоритов натрия и кальция) менее опасно в обслуживании и не требует сложных технологических решений. Однако используемое при этом реагентное хозяйство более громоздко, что связано с необходимостью хранения больших количеств препаратов (в 3–5 раз больше, чем при использовании хлора). Во столько же раз увеличивается объем перевозок. При хранении происходит частичное разложение реагентов с уменьшением содержания хлора. Остается необходимость устройства системы притяжно-вытяжной вентиляции и соблюдения мер безопасности для обслуживающего персонала. Растворы хлорсодержащих реагентов коррозионно-активны и требуют оборудования и трубопроводов из нержавеющих материалов или с антикоррозийным покрытием .
Вода – это фактор, который напрямую влияет на качество жизни человека. От ее цвета и запаха зависит настроение человека утром после умывания, а от состава – самочувствие и здоровье организма.
Вода, являясь основой жизни, легко распространяет инфекционные заболевания. Чтобы предотвратить передачу болезнетворных микроорганизмов через питьевую воду, применяют обеззараживание и дезинфекцию жидкости. Эти процессы позволяют уничтожить грибки, бактерии, неприятный привкус и цвет, что обеспечивает безопасность питьевой воды.
Очистка и обеззараживание питьевой воды для подачи в жилые дома проводится на станциях водоподготовки централизованного водоснабжения. Также существуют методы и установки для локального использования – в виде небольших систем очистки воды из скважины или способов, позволяющих очищать воду, набранную в бутылку.
Классификация методов обеззараживания воды
Чтобы правильно выбрать способ обеззараживания, проводят анализ загрязненной воды. Исследуется количество и вид микроорганизмов, степень побочной загрязненности. Также определяется объем воды, которая будет проходить очистку, и экономический фактор.
Вода, прошедшая очистку, прозрачна и бесцветна, не пахнет и не имеет вкуса и привкуса. Чтобы добиться такого эффекта, применяют следующие группы методов:
- физические;
- химические;
- комбинированные.
Каждой группе присущи свои отличительные признаки, но все методы так или иначе позволяют удалить патогенные микроорганизмы из воды. Получить подробную информацию по оборудованию для очистки и обеззараживания воды можно в компании «КВАНТА+» в г. Тюмень.
Химический метод – это работа с реагентами, добавляемыми в воду. Физическое обеззараживание выполняется за счет температуры или различных излучений. Комбинированные методы сочетают работу этих двух групп.
Наиболее эффективные способы
Инфекционная безопасность воды – это важная и актуальная проблема, из-за чего изобретено множество методик для избавления воды от микроорганизмов. Способы дезинфекции не прекращают улучшаться. Они становятся более результативными и доступными. В наше время самыми лучшими считаются следующие методы:
- термообработка с помощью высоких температур;
- ультразвуковая обработка;
- реагентные методы;
- ультрафиолетовое облучение жидкости;
- высокомощные электрических разрядов.
Физические методы обеззараживания воды
Перед ними вода обязательно должна проходить очистку от взвесей и примесей. Для этого применяется коагуляция, сорбция, флотация и фильтрация.
К данному виду методов относится применение:
- ультразвука;
- ультрафиолета;
- высоких температур;
- электричества.
Обеззараживание ультрафиолетом
Дезинфицирующее действие ультрафиолетового излучения известно очень давно. Его работа сходна с солнечным светом, успешно уничтожающим неприспособленные микроорганизмы за пределами озонового слоя Земли. Ультрафиолет воздействует на клетки, создавая поперечные сшивки в ДНК, вследствие чего клетка теряет возможность делиться и погибает (Рис. 2).
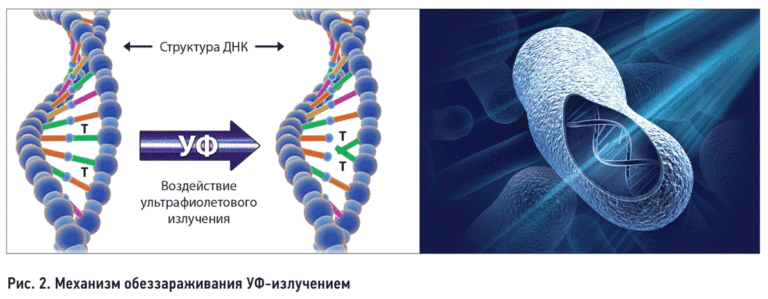 Установка состоит из ламп, помещенных в кварцевые чехлы. Лампы производят изучение, мгновенно уничтожающее микроорганизмы, а чехлы не позволяют лампам остывать. Качество обеззараживания при использовании этого метода зависит от прозрачности воды: чем чище поступающая жидкость, тем дальше распространяется свет и тем меньше загрязняется лампа. Для этого перед обеззараживанием вода проходит другие стадии очистки, в том числе механические фильтры.Резервуар, через который протекает вода, обычно оборудован мешалкой. Перемешивание слоев жидкости позволяет процессу дезинфекции проходить более равномерно.
Установка состоит из ламп, помещенных в кварцевые чехлы. Лампы производят изучение, мгновенно уничтожающее микроорганизмы, а чехлы не позволяют лампам остывать. Качество обеззараживания при использовании этого метода зависит от прозрачности воды: чем чище поступающая жидкость, тем дальше распространяется свет и тем меньше загрязняется лампа. Для этого перед обеззараживанием вода проходит другие стадии очистки, в том числе механические фильтры.Резервуар, через который протекает вода, обычно оборудован мешалкой. Перемешивание слоев жидкости позволяет процессу дезинфекции проходить более равномерно.
 Конструкция установки УФ-обеззараживания
Конструкция установки УФ-обеззараживания
Важно знать, что лампы и чехлы требуют регулярного ухода: конструкцию необходимо разбирать и очищать не менее одного раза в квартал.
Тогда результативность процесса не будет ухудшаться из-за появления накипи и других загрязнений. Сами лампы подлежат замене раз в год.
Установки ультразвукового обеззараживания
Работа таких установок основана на кавитации. Из-за интенсивных колебаний, которым подвергается вода благодаря высокочастотному звуку, в жидкости образуются многочисленные пустоты, она будто «вскипает». Мгновенный перепад давлений приводит к разрыву клеточных оболочек и гибели микроорганизмов.
Оборудование для ультразвуковой обработки воды эффективно, но требует больших затрат и грамотной эксплуатации. Важно, чтобы персонал умел обращаться с устройством – от качества настройки оборудования зависит его результативность.
Термическое обеззараживание
Этот метод крайне распространен среди населения и активно применяется в быту. С помощью высокой температуры, то есть кипячения, вода очищается практически от всех возможных патогенных организмов. В дополнение к этому снижается жесткость воды и уменьшается содержание растворенных газов. Вкусовые качества воды остаются прежними. Однако, у кипячения есть один недостаток: вода считается безопасной около суток, после чего бактерии и вирусы вновь могут в ней обосноваться.
 Кипячение воды – надежный и простой метод обеззараживания
Кипячение воды – надежный и простой метод обеззараживания
Электроимпульсное обеззараживание
Методика заключается в следующем: электрические разряды, поступающие в воду, создают ударную волну, микроорганизмы попадают под гидравлический удар и погибают. Этот способ не требует предварительной очистки и эффективен даже при повышенной мутности. Гибнут не только вегетативные, но и спорообразующие бактерии. Преимуществом является длительное сохранение эффекта (вплоть до 4-х месяцев), а недостатком – немалая стоимость и большое энергопотребление.
Химические методы обеззараживания воды
Они основаны на химических реакциях, которые происходят между загрязнением или микроорганизмом и добавляемым в жидкость реагентом.
При химическом обеззараживании важно контролировать дозу реагента.
Она должна быть точной. Недостаток вещества не сможет исполнить свою цель. К тому же, небольшое количество реагента приведет к повышенной активности вирусов и бактерий.
Чтобы улучшить работу химиката, его добавляют с избытком. В таком случае вредоносные микроорганизмы погибают, а эффект сохраняется продолжительное время. Избыток рассчитывается отдельно: если добавить слишком много, реагент дойдет до потребителя, и он отравится.
Хлорирование
Хлор широко распространен и применяется в водоочистке многих стран мира. Он успешно справляется с любыми объемами микробиологических загрязнений. Хлорирование приводит к гибели большей части патогенных организмов и отличается дешевизной и доступностью. К тому же, использование хлора и его соединений позволяет извлекать из воды металлы и сероводород. Хлорирование применяется в городских системах подачи питьевой воды. Оно также используется в бассейнах, где скапливается большое число людей.
 Однако, у этого способа есть ряд недостатков. Хлор крайне опасен, вызывает рак и клеточные мутации, токсичен. Если избыток хлора не исчезнет в трубопроводе, а дойдет до населения, это может привести к серьезным проблемам со здоровьем. Особенно сильна опасность в переходные периоды (осень и весну), когда из-за увеличения загрязненности поверхностных вод повышают дозу реагента при водоподготовке. Кипячение такой воды не поможет избежать негативных последствий, а наоборот – хлор превратится в диоксин, являющийся сильнейшим ядом. Для того, чтобы дать излишку хлора испариться, воду из-под крана набирают в большие емкости и оставляют на сутки в хорошо проветриваемом помещении.
Однако, у этого способа есть ряд недостатков. Хлор крайне опасен, вызывает рак и клеточные мутации, токсичен. Если избыток хлора не исчезнет в трубопроводе, а дойдет до населения, это может привести к серьезным проблемам со здоровьем. Особенно сильна опасность в переходные периоды (осень и весну), когда из-за увеличения загрязненности поверхностных вод повышают дозу реагента при водоподготовке. Кипячение такой воды не поможет избежать негативных последствий, а наоборот – хлор превратится в диоксин, являющийся сильнейшим ядом. Для того, чтобы дать излишку хлора испариться, воду из-под крана набирают в большие емкости и оставляют на сутки в хорошо проветриваемом помещении.
Озонирование
Озон обладает сильным окисляющим воздействием. Он проникает внутрь клетки и разрушает ее стенки, приводя к гибели бактерии. Это вещество не только является сильным антисептиком, но также обесцвечивает и дезодорирует воду, окисляет металлы. Озон работает быстро и избавляется практически от всех микроорганизмов, находящихся в воде, обгоняя по этой характеристике хлор.
Озонирование считается наиболее безопасным и эффективным методом, но и оно имеет несколько минусов. Избыток озона приводит к коррозии металлических частей оборудования и трубопроводов, аппараты изнашиваются и разрушаются быстрее обычного. Кроме того, новейшие исследования отмечают, что озонирование вызывает «пробуждение» микроорганизмов, находившихся в условной спячке.
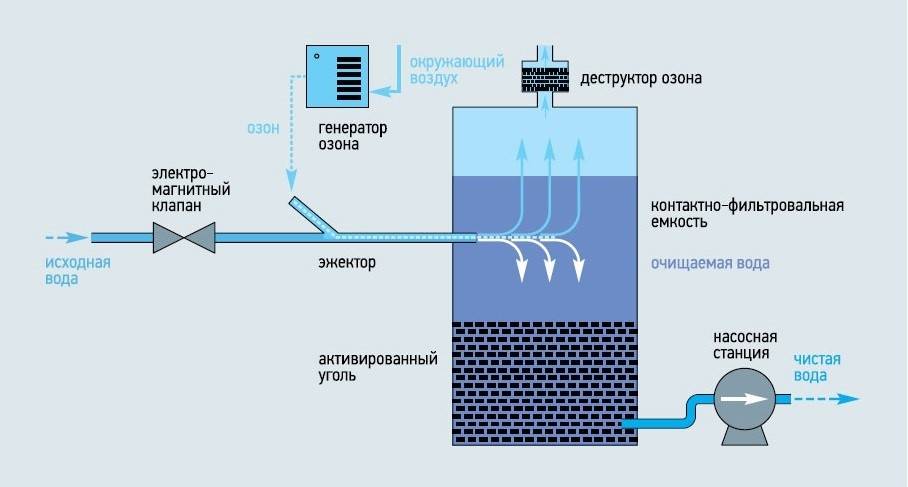 Схема процесса озонирования
Схема процесса озонирования
Способ отличается дороговизной установки и большим энергопотреблением. Для работы с озонирующим оборудованием требуется персонал высокой квалификации, ведь газ токсичен и взрывоопасен. Чтобы пустить воду населению, необходимо переждать период распада озона, иначе могут пострадать люди.
Обеззараживание полимерными соединениями
Отсутствие вреда здоровью, уничтожение запахов, вкусов и цветности, большая длительность действия – перечисленные достоинства относятся к обеззараживанию с помощью полимерных реагентов. Такой вид веществ также называют полимерными антисептиками. Они не вызывают коррозию и не портят ткань, не вызывают аллергии и отличаются результативностью.
 Олигодинамия
Олигодинамия
Она основана на способности благородных металлов (таких как золото, серебро и медь) обеззараживать воду.
То, что эти металлы имеют антисептический эффект, известно давно. Медь и её сплавы часто применяют в полевых условиях, когда нужно в индивидуальном порядке обеззаразить небольшой объем жидкости.
Для более обширного воздействия металлов на микроорганизмы используются ионаторы. Это проточные аппараты, работающие на основе гальванической пары и электрофореза.
Обеззараживание серебром
Этот металл принято считать одним из самых древних способов обеззараживания воды. В древности было распространено мнение, что серебро лечит от любых болезней. Сейчас известно, что оно негативно влияет на множество микроорганизмов, однако неизвестно, уничтожает ли серебро простейшие бактерии.
Данное средство дает видимый эффект при очистке воды. Однако оно негативно влияет на организм человека при накоплении в нем. Не зря серебро имеет высокий класс опасности. Обеззараживание воды ионами серебра не считается безопасным методом, а потому практически не используется в промышленности. Серебряные ионаторы используются в единичных случаях в быту для обработки небольших объемов воды.
 Компактный бытовой ионатор (осеребритель) воды
Компактный бытовой ионатор (осеребритель) воды
Иодирование и бромирование
Йод широко известен и используется в медицине с давних времен. Ученые многократно пытались использовать его обеззараживающее воздействие в водоочистке, однако его применение приводит к возникновению неприятного запаха. Бром отлично справляется практически со всеми известными патогенными микроорганизмами. Но имеет существенный недостаток – высокую стоимость. Из-за своих минусов эти два вещества для обработки сточных и питьевых вод не используются.
Комбинированные методы обеззараживания воды
Комплексные методы основываются на сочетании физических и химических методов для улучшения результативности. Примером является комбинация из ультрафиолетового излучения и хлорирования (иногда хлорирование заменяется на озонирование). УФ-лампы уничтожают микроорганизмы, а хлор или озон предотвращают их повторное возникновение. Кроме того, хорошо сочетаются окисление и обработка тяжелыми металлами. Реагент-окислитель дезинфицирует, а металлы продлевают бактерицидное действие.
 Сочетание УФ-обеззараживания и действия ультразвука
Сочетание УФ-обеззараживания и действия ультразвука
Как обеззаразить воду в быту
Существует пять способов быстро продезинфицировать небольшой объем воды:
- кипячение;
- добавление перманганата калия;
- использование обеззараживающих таблеток;
- использование трав и цветов;
- настаивание с кремнием.
Перманганат калия прибавляется воду в количестве 1-2 г. на одно ведро воды, после чего загрязнения выпадают в осадок.
Специальные таблетки для уничтожения микроорганизмов применяются при обезвреживании воды из скважины, колодца или родника. Они являются наиболее современным способом, доступным, недорогим и результативным. Многие таблетки, например, марки «Акватабс», могут использоваться для очистки больших объемов жидкости.
Если воду необходимо обеззаразить в походе, можно воспользоваться специальными травами: зверобоем, брусникой, ромашкой или чистотелом.
Также можно использовать кремний: его помещают в воду и оставляют на сутки.
Нормативная документация в области безопасности питьевой воды
Со стороны государства качество воды строго контролируется с помощью нормативных документов, правил и ограничений. Основой законодательных актов в области охраны водных ресурсов и контроля качества используемой воды являются два документа: Федеральный закон «О санитарно-эпидемиологическом благополучии населения» и Водный кодекс.
Первый закон содержит требования к качеству источников водоснабжения, из которых вода поступает в жилые дома и на нужды сельского хозяйства. Второй документ описывает нормы использования водных источников и указания по обеспечению их безопасности, а также определяет меры наказания.
ГОСТы
ГОСТы описывают правила, по которым должен проходить контроль качества сточных и питьевых вод. В них содержатся методики проведения анализов в полевых условиях, а также позволяют разделить воды на группы. Самые важные из ГОСТов представлены в таблице.
СНиПы
Строительные нормы и правила определяют требования к возведению сооружений очистки вод, к монтажу различных видов трубопроводов и систем водоснабжения. Информация содержится в СНиПах под следующими номерами: СНиП 2.04.01-85, СНиП 3.05.01-85, СНиП 3.05.04-85.
СанПиНы
Санитарно-эпидемиологические правила и нормы содержат гигиенические требования к качеству различных групп вод, к составу, к водозаборным сооружениям и месторасположению водозаборов: СанПиН 2.1.4.559-96, СанПиН 4630-88, СанПиН 2.1.4.544-96, СанПиН 2.2.1/2.1.1.984-00.
Таким образом, эффективность обеззараживания водопроводной воды контролируется с установленной регулярностью и в соответствии со множеством правил и нормативов. А большое число различных методов дезинфекции свежей воды позволяют для любых условий подобрать оптимальный вариант. Что делает грамотно очищенную и обработанную воду безопасной для употребления людьми.
Введение
Природная вода, как правило, не соответствует гигиеническим требованиям, предъявляемым к питьевой воде, поэтому перед подачей населению практически всегда необходима ее очистка и обеззараживание. Потребляемая человеком для питья, как и используемая на различных производствах, природная вода должна быть безопасной в санитарно-эпидемиологическом отношении, безвредной по своему химическому составу и иметь благоприятные органолептические свойства.
Известно, что ни один из современных методов обработки воды не обеспечивает ее 100 %-ной очистки от микроорганизмов. Но даже если бы система водоподготовки и могла способствовать абсолютному удалению из воды всех микроорганизмов, то всегда остается большая вероятность вторичного загрязнения очищенной воды при ее транспортировке по трубам, хранении в емкостях, контакте с атмосферным воздухом и т. д.
Санитарные правила и нормы (СанПиН) не ставят целью доведение воды по микробиологическим показателям до идеального, а следовательно, стерильного качества, при котором в ней будут отсутствовать все микроорганизмы. Задача состоит в том, чтобы удалить наиболее опасные из них для здоровья человека.
Основными документами, которые определяют гигиенические требования к качеству питьевой воды, являются: СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества» и СанПиН 2.1.4.1175-02 «Питьевая вода и водоснабжение населенных мест. Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников».
В настоящее время известно много методов обеззараживания воды и множество приборов, использующихся их для реализации. Выбор способа обеззараживания зависит от множества факторов: источника водоснабжения, биологических особенностей микроорганизмов, экономической целесообразности и т. д.
Главная задача этого издания – дать основные сведения о современных методах обеззараживания воды для питьевых целей, краткую характеристику каждого метода, аппаратурного его оформления и возможности применения в практике централизованного и индивидуального водоснабжения.
Важно и нужно, чтобы каждый водопользователь мог правильно сформулировать цели и задачи при выборе метода обеззараживая и в конечном итоге – получения качественной питьевой воды.
В издании приведены начальные сведения по основным источникам водопользования, их характеристика и данные о пригодности источника для питьевых целей, а также нормативные документы, регламентирующие водно-санитарное законодательство, сравнительный обзор нормативных документов, регламентирующих качество питьевой воды в части обеззараживания, принятых в России и за рубежом.
Очистка воды, в том числе её обесцвечивание и осветление, является первым этапом в подготовке питьевой воды, на котором из нее удаляются взвешенные вещества, яйца гельминтов и значительная часть микроорганизмов. Однако некоторые патогенные бактерии и вирусы проникают через очистные сооружения и содержутся в фильтрованной воде.
Для того чтобы создать надёжный барьер на пути возможной передачи через воду кишечных инфекций и других, не менее опасных болезней, и применяется её обеззараживание, т. е. уничтожение патогенных микроорганизмов – бактерий и вирусов.
Именно микробиологические загрязнения воды приводят к максимальному риску для здоровья человека. Доказано, что опасность заболеваний от присутствующих в воде болезнетворных микроорганизмов в тысячи раз выше, чем при загрязнении воды химическими соединениями различной природы.
Исходя из вышеизложенного, можно сделать вывод, что именно обеззараживание до пределов, отвечающих установленным гигиеническим нормативам, является обязательным условием получения воды для питьевых нужд.
1. Источники водоснабжения, их пригодность для обеззараживания
Все источники водозабора подразделяются на два больших класса – подземные воды и поверхностные воды. К подземным относятся: артезианские, подрусловые, родниковая. Поверхностные воды – это речная, озерная, морская и вода из водохранилищ.
В соответствии с требованиями нормативного документа ГОСТ 2761-84, выбор источника водоснабжения производится на основании следующих данных:
при подземном источнике водоснабжения – анализов качества воды, гидрогеологической характеристики используемого водоносного горизонта, санитарной характеристики местности в районе водозабора, существующих и потенциальных источников загрязнения почвы и водоносных горизонтов;
при поверхностном источнике водоснабжения – анализов качества воды, гидрологических данных, минимальных и средних расходов воды, соответствия их предполагаемому водозабору, санитарной характеристики бассейна, развития промышленности, наличия и возможности появления источников бытового, промышленного и сельскохозяйственного загрязнения в районе предполагаемого водозабора. Характерной чертой воды из поверхностных источников является наличие большой водной поверхности, которая непосредственно соприкасается с атмосферой и находится под воздействием лучистой энергии солнца, что создает благоприятные условия для развития водной флоры и фауны, активного течения процессов самоочищения.
Однако вода открытых водоемов подвержена сезонным колебаниям состава, содержит различные примеси – минеральные и органические вещества, а также бактерии и вирусы, а вблизи крупных населенных пунктов и промышленных предприятий велика вероятность ее загрязнения различными химическими веществами и микроорганизмами.
Для речной воды характерны высокая мутность и цветность, наличие большого количества органических веществ и бактерий, низкое солесодержание и жесткость. Санитарные качества речной воды низкие вследствие загрязнения ее сточной водой из жилых поселков и городов.
Для озерной и воды из водохранилищ характерны низкое содержание взвешенных частиц, высокая цветность и перманганатная окисляемость, часто наблюдается цветение воды за счет развития водорослей. Озерная вода имеет различную степень минерализации. Эти воды небезопасны в эпидемиологическом отношении.
В поверхностных водотоках происходят процессы самоочищения воды за счет физических, химических и биологических реакций. Под действием биохимических процессов при участии простейших водных организмов, микробов-антагонистов, антибиотиков биологического происхождения погибают патогенные бактерии и вирусы.
Круговорот воды в глобальном природном цикле: 1– мировой океан; 2 – почвенные и грунтовые воды; 3 – поверхностные воды суши; 4 – снег и лед; 5 – транспирация; 6 – речной (поверхностный) сток; 7 – вода в атмосфере в виде паров и атмосферной влаги.
Как правило, процессы самоочищения не обеспечивают качества воды, необходимого для хозяйственно-питьевых нужд, поэтому вся поверхностная вода подвергается процессам очищения с обязательным последующим обеззараживанием.
Воды из подземных источников водозабора имеют ряд преимуществ перед поверхностными: защищенность от внешнего воздействия и безопасность в эпидемиологическом отношении.
Морская вода содержит большое количество минеральных солей. Ее применяют в производственном водоснабжении для охлаждения, а при отсутствии пресных вод – и для целей хозяйственно-питьевого водоснабжения после опреснения.
Применение воды из подземных источников водозабора для водоснабжения имеет ряд преимуществ перед поверхностными источниками. Самыми важными из них являются защищенность от внешнего воздействия и, как следствие, безопасность в эпидемиологическом отношении.
Накопление и движение подземных вод зависит от строения пород, которые по отношению к воде разделяются на водонепроницаемые (водоупорные) и водопроницаемые. К водонепроницаемым относятся: гранит, глина, известняк; к водопроницаемым – песок, гравий, галечник и трещиноватые породы.
По условиям залегания подземные воды делятся на почвенные, грунтовые и межпластовые.
Почвенные воды наиболее близко расположены к поверхности, не защищены ни одним водонепроницаемым слоем. И как результат состав почвенных вод испытывает сильные колебания состава как в кратковременные периоды (дождь, засуха и т. д.), так и по временам года, например, таяние снега. Так как атмосферные воды могут легко попадать в почвенные, то применение почвенных вод для водоснабжения требует системы очистки и обязательного обеззараживания.
Грунтовые воды расположены ниже почвенных, глубина залегания от двух до нескольких десятков метров; они скапливаются на первом водонепроницаемом слое, но не имеют верхнего водонепроницаемого слоя. Между грунтовыми и почвенными водами может происходить водообмен, поэтому качество почвенных вод влияет на состояние грунтовых. Состав грунтовых вод подвержен несильным колебаниям и является фактически постоянным. В процессе фильтрования через слой почвы воды очищаются от минеральных примесей и частично от бактерий и микроорганизмов. Грунтовые воды являются наиболее распространенными источниками водоснабжения в сельских местностях.
Подрусловые воды – это воды, добываемые из скважин, глубина которых соответствует отметкам дна ручья, реки или озера. Может происходить просачивание речной воды в грунтовый слой, эти воды также называют подрусловыми. Состав подрусловых вод подвержен различным колебаниям, не очень надежен в санитарном отношении; и применение этих вод для системы водоснабжения требует очистки и обеззараживания.
Родник – это источник воды, самостоятельно изливающийся на поверхность. Наличие родника свидетельствует о нахождении в глубине водоупорного слоя, подпирающего водоупорный пласт, насыщенный влагой. Качество и состав родниковой воды определяется питающей ее грунтовой водой.
Межпластовые воды находятся между двумя водонепроницаемыми породами. Верхний водонепроницаемый слой защищает эти воды от проникновения атмосферных осадков и грунтовых вод. Вследствие глубокого залегания колебания состава воды незначительные, воды наиболее благополучные в санитарном отношении.
Загрязнение межпластовых вод происходит крайне редко: только при нарушении целостности водоупорных слоев или при отсутствии надзора за старыми скважинами, бывшими в эксплуатации на протяжении долгого времени.
Межпластовые воды могут иметь естественный выход на поверхность в виде восходящих ключей или родников – эти воды более всего подходят для системы питьевого водоснабжения.
Следует отметить, что единого состава воды не существует, поскольку даже артезианская вода, залегающая на одной и той же глубине, попадает к нам в дом, проходя через различные породы, изменяя при этом свой состав.
2. Классификация методов обеззараживания
В технологии водоподготовки существует много методов обеззараживания воды, которые условно можно разделить на два основных класса – химические и физические, а также их комбинирование.
В химических методах обеззараживание достигается введением в воду биологически активных соединений.
При физических методах вода подвергается обработке различными физическими воздействиями.
К химическим или реагентным методам обеззараживания воды относится введение сильных окислителей, в качестве которых используют хлор, диоксид хлора, озон, иод, гипохлорит натрия и кальция, перекись водорода, марганцевокислый калий. Из вышеперечисленных окислителей практическое применение в системах обеззараживания воды находят: хлор, озон, гипохлорит натрия, диоксид хлора. Другой химический метод – олигодинамия – воздействие на воду ионами благородных металлов.
В случае обеззараживания питьевой воды химическим методом для достижения стойкого обеззараживающего эффекта необходимо правильно определить дозу вводимого реагента и обеспечить достаточную длительность его контакта с водой. Доза реагента при этом рассчитывается, или проводится пробное обеззараживание на модельном растворе/объекте.
Доза реагента рассчитывается с избытком (остаточный хлор), гарантирующим уничтожение микроорганизмов, даже попадающих в воду еще на протяжении некоторого времени после ее обеззараживания, что обеспечивает пролонгированный эффект.
Физические методы обеззараживания:
– ультрафиолетовое облучение;
– термическое воздействие;
– ультразвуковое воздействие;
– воздействие электрическим разрядом.
При физических методах обеззараживания воды к единице её объема необходимо подвести заданное количество энергии, определяемое как произведение интенсивности воздействия (мощности излучения) на время контакта.
Эффективность обеззараживания воды химическими и физическими методами во многом зависит от свойств воды, а также от биологических особенностей микроорганизмов, т. е. их устойчивости к этим воздействиям.
Выбор метода, оценка экономической целесообразности применения того или иного метода обеззараживания воды определяется источником водоснабжения, составом воды, типом установленного оборудования водопроводной станции и ее местоположением (удаленностью от потребителей), стоимостью реагентов и оборудования дезинфекции.
Важно понимать – ни один из методов обеззараживания не является универсальным и самым лучшим. Каждый метод обладает своими достоинствами и недостатками.
3. Нормативно-технические документы водно-санитарного законодательства
Вода, потребляемая людьми, живущими в самых различных условиях, поступает из многих источников. Это могут быть реки, озера, болота, водоёмы, колодцы, артезианские скважины и т. д. Соответственно, вода, добываемая из разных по происхождению источников, различается по своим качествам и свойствам.
Существует большая вероятность того, что даже вода из близко расположенных друг к другу источников будет разительно различаться по качеству.
Промышленные предприятия, санатории, коммерческие компании, больницы и прочие лечебные учреждения, сельские жители и жители мегаполисов – все предъявляют свои, особые, требования к качеству воды.
Именно поэтому очистка и обеззараживание воды необходимы тогда, когда качество воды не отвечает требованиям потребителей.
Требования к качеству и безопасности воды установлены в следующих основных нормативных документах, перечисленных в табл. 1.
Таблица 1
Существуют также технологические нормативы и требования, связанные с проектированием систем водоподготовки (табл. 2).
Таблица 2
Безопасность воды в эпидемическом отношении определяется общим числом микроорганизмов и числом бактерий группы кишечных палочек. По микробиологическим показателям вода должна соответствовать требованиям, приведенным в табл. 3.
Таблица 3
*Индикаторные параметры качества воды. Только в целях мониторинга государства – члены ЕС на своей территории или ее части могут устанавливать дополнительные параметры, но их введение не должно ухудшать здоровье людей.
**Обязательные параметры.
4. Обработка воды сильными окислителями
Обеззараживание воды реагентными методами осуществляется добавлением в воду различных химических дезинфицирующих средств или проведением специальных мероприятий. Применение химических веществ в обработке воды обычно приводит к образованию побочных химических продуктов. Однако риск для здоровья от их воздействия ничтожен по сравнению с риском, связанным с вредоносными микроорганизмами, развивающимися в воде вследствие отсутствия ее обеззараживания или его некачественного проведения.
Минздравом разрешено применение более 200 средств для дезинфекции и стерилизации воды.
В данном разделе рассмотрим основные дезинфектанты, применяемые в системах водоснабжения России.
4.1. Хлорирование
Хлор был открыт шведским химиком Шееле в 1774 г. С этого года начинется история применения реагентов, содержащих активный хлор (уже более двух веков). Почти сразу было обнаружено его отбеливающее действие на растительные волокна – лен и хлопок. После этого открытия в 1785 г. французский химик Клод Луи Бертолле использовал хлор для беления тканей и бумаги в промышленном масштабе.
Но только в XIX в. было обнаружено, что «хлорная вода» (так в то время называли результат взаимодействия хлора с водой) обладает и дезинфицирующим действием. Можно считать, что в качестве дезинфицирующего средства хлор начал применяться с 1846 г., когда в одном из госпиталей Вены для врачей была введена практика ополаскивать руки «хлорной водой».
В 1888 г. на Международном гигиеническом конгрессе в Вене было признано, что многие заразные болезни могут распространяться посредством питьевой воды, в том числе такая опасная и распространенная на тот период, как холера. Фактически этот конгресс послужил толчком для поиска наиболее эффективного способа обеззараживания воды. Развитие темы хлорирования для обеззараживания питьевой воды связано со строительством водопроводов в больших городах. Впервые для этой цели его применили в Нью-Йорке в 1895 г. В России хлор для обеззараживания питьевой воды первый раз был использован в начале XX в. в Петербурге.
В настоящее время наиболее распространенным методом обеззараживания воды является применение хлора и его соединений. Более 90 % воды (подавляющее большинство) подвергается хлорированию. Технологическая простота процесса хлорирования и доступность реагентов обеспечили широкое внедрение хлорирования в практику водоснабжения.
Самое главное преимущество этого способа обеззараживания – способность обеспечить микробиологическую безопасность воды в любой точке распределительной сети, в любой момент времени, при ее транспортировании пользователю – именно благодаря эффекту последействия. После введения хлорирующего агента в воду он очень долго сохраняет свою активность по отношению к микробам, угнетает их ферментные системы на всем пути следования воды по водопроводным сетям от объекта водоподготовки (водозабора) до каждого потребителя.
Благодаря окислительным свойствам и эффекту последействия, хлорирование предотвращает рост водорослей, способствует удалению из воды железа и марганца, разрушению сероводорода, обесцвечиванию воды, поддержанию микробиологической чистоты фильтров и т. п.
4.2. Методика хлорирования
При выборе метода хлорирования (обработки воды хлором или другими хлорагентами) необходимо учитывать целевое назначение процесса хлорирования, характер имеющихся в воде загрязнений, особенности колебания состава воды в зависимости от сезона. Особое внимание следует уделить специфическим особенностям технологической схемы очистки воды и оборудования, входящего в состав очистных сооружений.
По целям все методики можно разделить на два больших класса: первичное (предварительное хлорирование, предхлорирование) и финишное (окончательное) хлорирование.
Первичное хлорирование – введение хлора или хлорсодержащих реагентов в воду проводится максимально близко к источнику забора воды. По своим целям первичное хлорирование служит не только для обеззараживания воды, но и для интенсификации процессов очистки воды от примесей, например обезжелезивания, коагулирования. При этом используются большие дозы хлора, стадия дехлорирования, как правило, отсутствует, так как избыточное количество хлора полностью удаляется на других стадиях очистки воды.
Финишное или окончательное хлорирование – это процесс обеззараживания воды, проводимый как последняя стадия ее подготовки, т. е. предварительно все загрязняющие вещества уже удалены и хлор расходуется только на обеззараживание.
Хлорирование проводят как небольшими дозами хлора – нормальное хлорирование, так и повышенными дозами – перехлорирование.
Нормальное хлорирование применяют при заборе воды из надежных в санитарном отношении источников. Дозы хлора должны обеспечивать необходимый бактерицидный эффект без ухудшения органолептических показателей качества воды. Допустимое количество остаточного хлора после 30-минутного контакта воды с хлором – не выше 0,5 мг/л.
Перехлорирование применяется при заборе воды из источников, характеризующихся большими колебаниями состава, особенно по микробиологическим показателям, и в том случае, если нормальное хлорирование не дает стабильного бактерицидного эффекта. Также перехлорирование применяют при наличии в воде фенолов, когда нормальное хлорирование приводит только к ухудшению органолептических показателей качества воды. Перехлорирование устраняет многие неприятные привкусы, запахи и в некоторых случаях может применяться для очистки воды от токсичных веществ. Доза остаточного хлора при перехлорировании обычно устанавливается в пределах 1–10 мг/л. Избыток остаточного хлора затем удаляют дехлорированием воды; небольшой избыток – аэрированием; большее количество – добавками восстанавливающего реагента – дехлора (тиосульфата или сульфита натрия, дисульфита натрия, аммиака, сернистого ангидрида, активированного угля).
Комбинированные методы хлорирования, т. е. обработка воды хлором совместно с другими бактерицидными препаратами, используют для усиления действия хлора или фиксации его в воде на более длительный срок. Комбинированные методы хлорирования, как правило, применяют для обработки больших количеств воды на стационарных водопроводах. К комбинированным методам относятся: хлорирование с манганированием, хлорсеребряный и хлормедный способы, а также хлорирование с аммонизацией.
Несмотря на то что хлорирование до сих пор является самым распространенным методом обеззараживания, данному методу присущи и некоторые ограничения в применении, например:
– в результате хлорирования в обрабатываемой воде могут образоваться хлорорганические соединения (ХОС);
– традиционные способы хлорирования в некоторых случаях не являются барьером на пути проникновения ряда бактерий и вирусов в воду;
– хлорирование воды, проводимое в больших масштабах, вызвало широкое распространение резистивных к хлору микроорганизмов;
– растворы хлорсодержащих реагентов коррозионно активны, что порой является причиной быстрого износа оборудования;
Комбинированные методы хлорирования, обработка воды хлором совместно с другими бактерицидными препаратами, используют для усиления действия хлора или фиксации его в воде на более длительный срок.
В целях обеспечения здоровья населения во многих странах введены государственные нормативы, ограничивающие содержание ХОС в питьевой воде. В России нормируется 74 показателя, например:
– хлороформ – 0,2 мг/л;
– дихлорбромметан – 0,03 мг/л;
– четыреххлористый углерод – 0,006 мг/л.
В настоящее время предельно допустимые концентрации для веществ, являющихся побочными продуктами хлорирования, установлены в различных развитых странах в пределах от 0,06 до 0,2 мг/л, что соответствует современным научным данным о степени их опасности для здоровья.
Процесс образования ХОС довольно сложен, растянут по времени до нескольких часов и зависит от многих факторов: дозы хлора, концентрации в воде органических веществ, времени контакта, температуры, величины рН воды, щелочности и т. д. Главной причиной образования в воде ХОС является наличие органических гуминовых и фульвокислот, а также водорослевых метаболитов. Для устранения этих примесей впоследствии требуется доочистка воды угольными фильтрами. Наиболее интенсивное образование ХОС происходит при предварительном хлорировании, когда большие дозы хлора подаются в неочищенную воду, содержащую значительное количество органических веществ. В настоящее время существуют два основных метода предупреждения образования ХОС: коррекция схемы хлорирования и отказ от применения хлора как основного метода обеззараживания воды.
При коррекции схемы хлорирования осуществляется перенос места ввода основной части хлора в конец технологической схемы водоподготовки, что позволит отказаться от подачи больших доз хлора в неочищенную воду. При выборе данной схемы важным требованием является удаление органических соединений (предшественников образования ХОС) до ввода хлора. Отказа от предварительного хлорирования и переноса подачи основной дозы хлора в конец очистных сооружений обычно вполне достаточно для решения проблемы, связанной с образованием ХОС. Однако это приводит к значительному снижению эффективности обеззараживания воды и уменьшению значения очистных сооружений в качестве барьера.
Хлорирование воды является надежным средством, предотвращающим распространение эпидемий, так как большинство патогенных бактерий (бациллы брюшного тифа, туберкулеза и дизентерии, вибрионы холеры, вирусы полиомиелита и энцефалита) весьма нестойки в хлоре.
Об исключении хлора на первичном обеззараживании уместно говорить лишь при наличии в воде органических соединений, которые при взаимодействии с хлором (и гипохлоритом) образуют тригалометаны, негативно влияющие на организм человека.
Для хлорирования воды используются такие вещества, как собственно хлор (жидкий или газообразный), гипохлорит натрия, диоксид хлора и другие хлорсодержащие вещества.
4.2.1. Хлор
Хлор является самым распространенным веществом, используемым для обеззараживания питьевой воды. Это объясняется его высокой эффективностью, простотой используемого технологического оборудования, дешевизной применяемого реагента – жидкого или газообразного хлора – и относительной простотой обслуживания.
Хлор легко растворяется в воде, после смешения газообразного хлора с водой в водном растворе устанавливается равновесие:
НСlО Н + + ОСl -
Наличие хлорноватистой кислоты в водных растворах хлора и получающиеся в результате ее диссоциации анионы ОСl - обладают сильными бактерицидными свойствами. Хлорноватистая кислота почти в 300 раз более активна, чем гипохлорит-ионы ClO - . Объясняется это уникальной способностью HClO проникать в бактерии через их мембраны. Хлорноватистая кислота подвержена разложению на свету:
2HClO -> 2O + 2HCl -> О 2 + 2HCl
с образованием хлористоводородной кислоты и атомарного кислорода в качестве промежуточного вещества, который также является сильнейшим окислителем.
Обработку воды хлором осуществляют с помощью, так называемых, хлораторов, в которых газообразный (испаренный) хлор абсорбируют водой. Полученная хлорированная вода из хлоратора сразу подается к месту ее потребления. Несмотря на то что этот метод обработки воды и является наиболее распространенным, у него тоже есть ряд недостатков. Прежде всего, сложная транспортировка и хранение больших объемов жидкого высокотоксичного хлора. При такой организации процесса неизбежно присутствуют потенциально опасные стадии – прежде всего разгрузка емкостей с жидким хлором и его испарение для перевода в рабочую форму.
Создание рабочих запасов хлора на складах представляет опасность не только для рабочего персонала станции, но и для жителей расположенных рядом домов. Как альтернативный вариант хлорирования в последние годы все шире используют обработку воды раствором гипохлорита натрия (NaClO), этот метод находит применение как на промышленных станциях водоподготовки, так и на небольших объектах, в том числе в частных домах.
4.2.2. Диоксид хлора
Диоксид хлора применяют для обеззараживания воды в Европе, США и России. В США в 1944 г. была введена в эксплуатацию одна из первых систем обеззараживания питьевой воды диоксидом хлора – система «Ниагара Фоллз». В Германии используют диоксид хлора с 1959 г. Мировой опыт применения диоксида хлора и многочисленные исследования показали его эффективность при подготовке и дезинфекции питьевых, производственных и сточных вод.
Основные способы получения диоксида хлора
Распространены три основных метода получения диоксида хлора:
– взаимодействие хлорита натрия с соляной кислотой:
5NaClO 2 + 4HCl = 4ClO 2 + 5NaCl + 2H 2 O;
– взаимодействие хлорита натрия с молекулярным хлором, (гипохлоритом натрия, хлорноватистой кислотой). Реакция проводится путем введения газообразного хлора в раствор хлорита натрия в условиях вакуума:
2NaClO 2 + Cl 2 = 2ClO 2 + 2NaCl;
– взаимодействие хлората натрия с серной кислотой и перекисью водорода:
2NaClO 3 + H 2 SO 4 + 2H 2 O = 2ClO 2 + 2O 2 + Na 2 SO 4
Эффективное действие ClО 2 обусловлено не только высоким содержанием при реакции высвобождающегося хлора, но и образующимся атомарным кислородом.
В настоящее время есть установки, использующие все эти способы получения диоксида хлора для его дальнейшего применения в процессах обеззараживания питьевой воды. Основным фактором, мешающим широкому распространению использования диоксида хлора, является его повышенная взрывоопасность, осложняющая производство, транспортировку и хранение. Современные технологии устранили этот недостаток за счет производства диоксида хлора непосредственно на месте применения в виде водного раствора безопасной концентрации. Процессы получения и дозирования диоксида хлора в обрабатываемую воду полностью автоматизированы, не требуется присутствия обслуживающего персонала. В связи с этим возможно его применение в установках относительно небольшой производительности.
Применение диоксида хлора для обеззараживания воды обладает рядом преимуществ:
– диоксид хлора не образует тригалометанов при взаимодействии с органическими веществами, при этом способствует снижению концентраций железа и марганца в воде;
– является эффективным окислителем и дезинфектантом для всех видов микроорганизмов, включая цисты (Giardia, Cryptosporidium), споровые формы бактерий и вирусы;
– дезинфицирующее действие практически не зависит от pH воды, в то время как эффективность хлора снижается с отклонением значения pH от pH=7,4;
– дезодорирует воду, разрушает фенолы – источники неприятного вкуса и запаха;
– не образует броматов и броморганических побочных продуктов дезинфекции в присутствии бромидов.
Основным недостатком применения диоксида хлора является образование побочных продуктов – хлоратов и хлоритов, содержание которых в питьевой воде необходимо контролировать. В соответствии с СанПиН, предельно допустимая концентрация хлоритов – 0,2 мг/дм 3 с санитарно-токсикологическим лимитирующим показателем, соответствующим третьему классу опасности. Эти нормы ограничивают предельную дозу диоксида при дезинфекции воды.
4.2.3. Гипохлорит натрия
В качестве альтернативного варианта в последние годы все шире используют обработку воды раствором гипохлорита натрия (NaClO), причем этот реагент находит применение как на больших станциях водоподготовки, так и на небольших объектах, в том числе и в частных домах.
Водные растворы гипохлорита натрия получают химическим:
Cl 2 + 2NaOH = NaClO + NaCl + H 2 O
или электрохимическим методом по реакции:
NaCl + H 2 O = NaClO + H 2 .
Вещество гипохлорит натрия (NaClO) в чистом химическом виде (т. е. без воды) представляет собой бесцветное кристаллическое вещество, легко разлагающееся на хлорид натрия (поваренная соль) и кислород:
2NaClO = 2NaCl + O 2 .
При растворении в воде, гипохлорит натрия диссоциирует на ионы:
Гипохлорит-ион OCl - в воде подвергается гидролизу, образуя хлорноватистую кислоту HOCl:
ОCl - + H 2 O = HOCl + OH - .
Именно наличие хлорноватистой кислоты в водных растворах гипохлорита натрия объясняет его сильные дезинфицирующие и отбеливающие свойства. Наивысшая бактерицидная способность гипохлорита проявляется в нейтральной среде, когда концентрации HClO и гипохлорит-анионов ClO - приблизительно равны.
Разложение гипохлорита сопровождается образованием ряда активных частиц, в частности, атомарного кислорода, обладающего высоким биоцидным действием. Образующиеся частицы принимают участие в уничтожении микроорганизмов, взаимодействуя с биополимерами в их структуре, способными к окислению. Исследованиями установлено, этот процесс аналогичен тому, который происходит естественным образом во всех высших организмах. Некоторые клетки человека (нейтрофилы, гепатоциты и др.) синтезируют хлорноватистую кислоту и сопутствующие высокоактивные радикалы для борьбы с микроорганизмами и чужеродными субстанциям.
Обеззараживание воды и окисление примесей с использованием гипохлорита натрия, производимого электрохимически, впервые было применено в США в конце 30-х гг. XX в… Гипохлорит натрия обладает рядом ценных свойств. Его водные растворы не имеют взвесей и поэтому не нуждаются в отстаивании в противоположность хлорной извести. Применение гипохлорита натрия для обработки воды не вызывает увеличения ее жесткости, поскольку не содержит солей кальция и магния как хлорная известь или гипохлорит кальция.
Бактерицидный эффект раствора NaClO, полученного электролизом, выше, чем у других дезинфектантов, действующее начало которых – активный хлор. Кроме того, раствор обладает еще большим окислительным действием, чем растворы, приготовленные химическим методом, поскольку содержит больше хлорноватистой кислоты (HClO).
Недостатком данного метода является то, что водные растворы гипохлорита натрия неустойчивы и со временем разлагаются даже при комнатной температуре.
Промышленностью нашей страны гипохлорит натрия выпускается в виде водных растворов различной концентрации.
В соответствии с ГОСТ 11086-76 раствор гипохлорита натрия, получаемый по химическому методу, выпускается в виде трех марок. Ниже приведены показатели по составу продуктов.
Гипохлорит натрия в виде раствора (марки А, Б или «Белизна») – это раствор гипохлорита (16–19 % NaOCl) с примесью хлорида и гидроксида натрия (рН 12–14). Оба раствора со временем разлагаются. Скорость разложения зависит от условий их хранения.
Раствор гипохлорита натрия реагент легко дозируется, что позволяет автоматизировать процесс обеззараживания воды.
4.2.4. Хлорсодержащие реагенты
Использование для обеззараживания воды хлорсодержащих реагентов (хлорной извести, гипохлоритов натрия и кальция) менее опасно в обслуживании, чем применение хлора и не требует сложных технологических решений. Правда, применяемое при этом реагентное хозяйство более громоздко, что связано с необходимостью хранения больших количеств препаратов (в 3–5 раз больше, чем при использовании хлора). Во столько же раз увеличивается объем перевозок.
При хранении происходит частичное разложение реагентов с уменьшением содержания хлора. В связи с этим необходимо обустраивать систему притяжно-вытяжной вентиляции и соблюдать меры безопасности для обслуживающего персонала. Растворы хлорсодержаших реагентов коррозионно-активны и требуют оборудования и трубопроводов из нержавеющих материалов или с антикоррозийным покрытием, при индивидуальном водоснабжении обычно не используются.
4.2.5. Хлорирование для индивидуального водоснабжения
Все большее распространение, особенно на небольших станциях водоподготовки, получают установки по производству активных хлорсодержаших реагентов электрохимическими методами.
В России несколько предприятий предлагают установки типа «Санер», «Санатор», «Хлорэл-200» для производства гипохлорита натрия методом диафрагменного электролиза поваренной соли.
Наиболее просто и часто вопросы хлорирования воды для индивидуального водоснабжения решаются применением гипохлорита натрия, в качестве реагента возможно применение раствора «Белизна».
Многим потребителям не нравится то, что льющаяся из крана вода может иметь запах хлора, однако эта проблема легко решается посредством установки угольного фильтра.
Методы подготовки воды хлорированием требуют точного дозирования реагентов в обрабатываемую воду, поскольку реагенты отличаются высокой химической активностью. Для решения задач хлорирования нужно применять современную цифровую технику, обеспечивающую точное дозирование реагента пропорционально расходу или объему обрабатываемой воды.
На рынке представлено большое разнообразие дозирующих насосов, различающихся производительностью.
4.3. Другие галогены для обеззараживания воды
4.3.1. Йодирование
Йод – химический элемент из группы галогенов, «родственниками» которого являются фтор, хлор и бром, обозначается символом I (от греч. iodes – фиолетовый; лат Iodum), имеет порядковый номер 53, атомный – 126,90, плотность твердого – 4,94 г/см 3 , температура плавления – 113,5 °С, кипения – 184,35 °С. В природе йод в основном сосредоточен в морской воде (в среднем около 0,05 мг/л). Кроме того, он есть и в морских отложениях. Это позволяет ему переходить в подземные воды, в которых его содержание может достигать более 100 мг/л. Столь высокое содержание йода характерно также для районов нефтяных месторождений. В то же время в поверхностных водах его содержание невелико (концентрация колеблется от 1 до 0,01 мкг/л).
Как показывают исследования, метод йодирования эффективен в отношении бактерий и вирусов и недостаточно эффективен при воздействии на микробные токсины и фенольные соединения. Еще одно ограничение на распространение метода йодирования накладывает появление специфического запаха при растворении йода в воде. Поэтому йодирование воды в целях её обеззараживания не выдерживает конкуренции с традиционным хлорированием, несмотря на то, что йод, в отличие от хлора, имеет такие преимущества, как инертность по отношению к аммиаку и его производным, а также устойчивость к солнечной радиации. Обработка воды йодом для целей обеззараживания не нашла широкого распространения, хотя попытки йодирования водопроводной воды предпринимались неоднократно. В настоящее время обработка воды йодом применяется лишь при малых величинах расхода или в тех случаях, когда используются специальные схемы дезинфекции воды. Так, в ряде случаев йодом дезинфицируют воду в плавательных бассейнах.
Йод относится к числу микроэлементов, функции которых в организме весьма многообразны. Он участвует в синтезе гормонов щитовидной железы, воздействует на метаболические и регенерационные процессы. Недостаточное присутствие йода в организме приводит к негативным последствиям. Впрочем, опасность для здоровья человека несет не только недостаток йода, но и его избыток. Так, повышенное количество йода в организме приводит к изменению структурно-функциональных характеристик щитовидной железы, печени, почек.
Не так давно на рынке появились йодированные напитки и вода, расфасованные по бутылкам. Такой подход, несомненно, оправдан, поскольку только сам потребитель, руководствуясь медицинскими показаниями, может решить, стоит ему пить йодированную воду или нет.
В современной практике для обеззараживания питьевой воды йодированием предлагается использовать специальные иониты, насыщенные йодом. При прохождении через них воды йод постепенно вымывается из ионита, переходя воду. Такое решение возможно только для малогабаритных индивидуальных установок в бытовых системах доочистки воды. В таких системах йодирование воды проводится за счет дополнительной установки в одну из ступеней очистки специального фильтрующего элемента. Существенными недостатками являются изменение концентрации йода в процессе работы, невозможность точного дозирования в проточную воду и отсутствие контроля его концентрации.
На российском рынке представлены установки и картриджи «Гейзер» и «Чистая вода».
4.3.2. Бромирование
К химическим методам обеззараживания воды относится также применявшееся в начале XX в. обеззараживание соединениями брома, обладающими более выраженными бактерицидными свойствами, чем хлор, но требующими и более сложной технологии применения.
Бром – химический элемент из группы галогенов, обозначается символом Br (от греч. bromos – зловоние; название связано с неприятным запахом брома; лат. Bromum) имеет порядковый номер 35, атомный вес – 79,90, плотность жидкого – 3,11 г/см 3 , кипения – 59,2 °С.
Бром воздействует на микроорганизмы, убивает вирусы, бактерии, грибки, способствует удалению из воды органических примесей, эффективен в борьбе с водорослями. Соединения, основой которых является бром, устойчивы к солнечной радиации.
Однако несмотря на все свои преимущества, метод бромирования воды является очень дорогостоящим, поэтому он не получил широкого распространения при очистке питьевой воды и применяется в основном для обеззараживания воды в небольших бассейнах и СПА.
4.4. Озонирование
4.4.1. История озонирования
В 1840 г. немецкий ученый Шейнбейн, исследуя процессы разложения воды на водород и кислород при помощи электрической дуги, получил новый газ с резким специфическим запахом, который был им назван озоном. Затем были исследования других ученых по изучению свойств и применения озона. Изобретатель Н. Тесла запатентовал первый генератор озона в 1896 г.
Впервые процессы озонирования для очистки воды реализованы во Франции, где уже в 1907 г. был построен первый завод по озонированию воды в г. Бон Вуаяж (Франция) для нужд г. Ниццы, а в 1916 г. действовало 26 озонаторных установок (всего в Европе – 49).
В советское время озонирование было реализовано на Восточной водопроводной станции в Москве, станция была оснащена озонаторами французской компании «Трейли-газ».
4.4.2. Получение озона
Озон (O 3) – газ голубоватого или бледно-фиолетового цвета, самопроизвольно распадающийся на воздухе и в водном растворе, превращаясь в обычный кислород (О 2). Скорость распада озона резко увеличивается в щелочной среде и с ростом температуры. Доза озона зависит от назначения озонированной воды. Если речь идет об обеззараживании воды, предварительно прошедшей фильтрование и осветление, дозу озона принимают равной 1–3 мг/л, для подземной воды – 0,75–1 мг/л. При введении озона для обесцвечивания и обеззараживания загрязненной воды его необходимое количество может доходить до 5 г/л. Продолжительность контакта обеззараживаемой воды с озоном – 8–12 мин.
Озон образуется во многих процессах, сопровождающихся выделением атомарного кислорода, например при разложении перекисей, окислении фосфора и т. п.
Наиболее экономичный промышленный метод получения озона – воздействие на воздух или кислород электрическим разрядом 5000–25 000 В. Генератор озона состоит из двух установленных на небольшом расстоянии друг от друга пластинчатых или трубчатых (расположение концентрическое) электродов.
Сжижается O 3 легче, чем O 2 , и потому их несложно разделить. Озон для озонотерапии в медицине получают только из чистого кислорода. При облучении воздуха жёстким ультрафиолетовым излучением образуется озон. Те же процессы протекают в верхних слоях атмосферы, где под действием солнечного излучения образуется и поддерживается озоновый слой.
В лаборатории озон можно получить взаимодействием охлажденной концентрированной серной кислоты с пероксидом бария:
3H 2 SO 4 + 3BaO 2 = 3BaSO 4 + O 3 + 3H 2 O.
4.4.3. Обеззараживающее действие озона
При повышенном бактериальном загрязнении водоисточника или при наличии в нем патогенных микроорганизмов, энтеровирусов и цист лямблий, устойчивых к действию традиционного хлорирования, озон особенно эффективен. Механизм действия озона на бактерии полностью пока еще не выяснен, однако это не мешает его широкому использованию.
Озон гораздо более сильный окислитель, чем хлор (при применяемых дозах того и другого реагента).
По быстродействию озон эффективнее хлора: обеззараживание происходит быстрее в 15–20 раз. На споровые формы бактерий озон действует разрушающе, в 300–600 раз сильнее хлора. Это подтверждается сравнением их окислительных потенциалов: у хлора Cl 2 – 1,35 В, у озона О 3 – 1,95 В.
Отсутствие в воде химических веществ, быстро реагирующих с озоном, позволяет провести эффективное разрушение E.coli при концентрации растворенного озона 0,01–0,04 мг/л.
Для уничтожения бактерий полиомиелита (штамм Le и Mv) необходимо подвергать воду воздействию хлором в течение 1,5–3 ч при дозе окислителя 0,5–1 мг/л. В то же время озон разрушает эти бактерии за 2 мин при концентрации его в воде 0,05–0,45 мг/л.
Следует отметить такое важное свойство озона, как противовирусное воздействие. Энтеровирусы, в частности, выводящиеся из организма человека, поступают в сточные воды и, следовательно, часто могут попадать в воды поверхностных источников, используемых для питьевого водоснабжения.
Результатом многочисленных исследований установлено: остаточный озон в количестве 0,4–1,0 мг/л, сохраняемый в течение 4–6 мин, обеспечивает уничтожение болезнетворных вирусов, и в большинстве случае такого воздействия вполне достаточно, чтобы устранить все микробные загрязнения.
По сравнению с применением хлора, повышающем токсичность очищенной воды, определенной по гидробионтам, применение озона способствует снижению токсичности.
4.4.4. Аппаратурное оформление
Поскольку озон весьма токсичный газ (ПДК в воздухе зоны – 0,0001 г/м 3), схемы процессов озонирования воды предусматривают его полное использование и деструкцию. В состав озонаторного оборудования обычно входит и специальный дегазатор (деструктор) озона. Все установки озонирования смонтированы из коррозионностойких материалов, оборудованы запорной и сигнальной арматурой, оснащены автоматическими системами запуска (таймеры, реле давления, электромагнитные клапаны и т. д.) и защиты.
Метод озонирования воды технически сложен и наиболее дорогостоящ среди других методов обеззараживания питьевой воды. Технологический процесс включает последовательные стадии очистки воздуха, его охлаждения и осушки, синтеза озона, смешения озоновоздушной смеси с обрабатываемой водой, отвода и деструкции остаточной озоновоздушной смеси, вывода ее в атмосферу. Все это ограничивает использование данного метода в повседневной жизни.
На российском рынке бытовые озонаторы представлены моделями: «АкваМама», «Экотроника», «Озон Люкс» (RUIQI, состоит из озонатора и угольно фильтра) и др.
Озонаторные установки представлены оборудованием: станции озонирования воды серии CD-OWSG, серии СОВ-М, серии ПВО-TOG и ПВО-ZF, «Озон-ПВ» и др. Установки отличаются конструктивным исполнением и производительностью.
4.4.5. Особенности озонирования
С гигиенической точки зрения, озонирование – один из лучших способов обеззараживания питьевой воды. При высокой степени обеззараживания оно обеспечивает ее наилучшие органолептические показатели и отсутствие высокотоксичных и канцерогенных продуктов в очищенной воде.
Озон уничтожает известные микроорганизмы в 300–3000 раз быстрее, чем любые другие дезинфекторы. Озонирование не изменяет кислотность воды и не удаляет из неё необходимые человеку вещества. Остаточный озон быстро превращается в кислород (O 2) и обогащает им воду.
При озонировании не успевают возникнуть побочные вредные продукты реакции, по крайней мере, в заметных количествах.
Принципиальная технологическая схема озонирования воды: 1 – резервуар исходной воды; 2 – насос; 3 – массообменные аппараты; 4 – резервуар очищенной воды; 5 – генераторы озона; 6 – блок подготовки и сушки воздуха; 7 – деструктор озона (дегазатор).
Существуют некоторые недостатки применения озонирования, накладывающие соответствующие ограничения на его применение:
1. Метод озонирования технически сложен, требует больших расходов электроэнергии и использования сложной аппаратуры, для которой необходимо высококвалифицированное обслуживание.
2. Пролонгированное действие озона значительно меньше чем у хлора, благодаря его быстрому разрушению, поэтому повторное заражение воды при озонировании более вероятно, чем при хлорировании.
3. Озонирование может вызвать (особенно у высокоцветных вод и вод с большим количеством «органики») образование дополнительных осадков, поэтому нужно предусматривать после озонирования фильтрование воды через активный уголь. В результате озонирования образуются побочные продукты, включающие: альдегиды, кетоны, органические кислоты, броматы (в присутствии бромидов), пероксиды и другие соединения.
При воздействии на гуминовые кислоты, где есть ароматические соединения фенольного типа, может появиться и фенол.
Озон может вырабатываться только на месте потребления, поскольку его хранение и транспортировка невозможны. Для выработки озона нужен свободный газообразный кислород.
5. Олигодинамия
Олигодинамия – это воздействие ионов благородных металлов на микробиологические объекты. Говоря о олигодинамии, как правило, рассматривают три металла – золото, медь и серебро. Наиболее распространенным методом для практических целей является применение серебра, иногда используются бактерицидные растворы на основе меди. Золото не находит реального применения на практике, так как этот металл является очень дорогим.
5.1. Серебро
Серебро – химический элемент, относится к благородным металлам, обозачается символом Ag (от лат. Silver – светлый, белый, англ. Argentum, франц. Argent, нем. Silber). Имеет порядковый номер 47, атомный вес – 107,8, валентность – I. II, плотность – 10,5 г/см 3 , температура плавления – 960,5 °С, кипения – 2210 °С.
Несмотря на то, что серебряные руды разбросаны по всему миру (Австралия, Перу, Япония, Канада), основным поставщиком серебра является Мексика. Серебро – хороший проводник тепловой энергии.
5.1.1. История
Серебро известно человечеству с древнейших времён, в своё время его добывали в виде самородков, т. е. не приходилось выплавлять из руд, и многие народы считали его священным металлом, например в Ассирии и Вавилоне. В Европе по количеству серебра судили о состоянии королей. В средние века серебро и его соединения были очень популярны среди алхимиков. Позднее из серебра изготавливают посуду, чеканят монеты, делают ювелирные украшения, сейчас применяют при изготовлении электрических контактов и печатных схем, источников питания.
Бактерицидное действие серебра также известно с древнейших времен. В древних индусских трактатах встречается описание об обряде кратковременного погружения в емкость с водой раскаленного серебра.
Основоположником научного изучения механизма действия серебра на микробную клетку является швейцарский ученый Карл Негель, который в 80-е гг. XIX в. установил, что взаимодействие ионов серебра (а не самого металла) с клетками микроорганизмов вызывает их гибель. Это явление он назвал олигодинамией (от греч. «олигос» – малый, следовой и «динамос» – действие, т. е. действие следов). Немецкий ученый Винцент, сравнивая активность некоторых металлов, установил, что наиболее сильным бактерицидным действием обладает серебро, меньшим – медь и золото. Так, дифтерийная палочка погибала на серебряной пластинке через три дня, на медной – через шесть дней, на золотой – через восемь.
5.1.2. Описание метода
Большой вклад в изучение антимикробных свойств «серебряной» воды, ее применения для обеззараживания питьевой воды и пищевых продуктов внес академик Л. А. Кульский. Его экспериментами, а позднее и работами других исследователей доказано, что именно ионы металлов и их диссоциированные соединения (вещества, способные в воде распадаться на ионы) вызывают гибель микроорганизмов. Доказано, что чем выше концентрация ионов серебра, тем больше его активность и бактерицидный эффект.
Научно доказано, что серебро в ионном виде обладает бактерицидным, противовирусным, выраженным противогрибковым и антисептическим действием и служит высокоэффективным обеззараживающим средством в отношении патогенных микроорганизмов, вызывающих острые инфекции. Эффект уничтожения бактерий препаратами серебра очень велик. Он в 1750 раз сильнее действия концентрированной карболовой кислоты и в 3,5 раза сильнее действия сулемы. По данным академика Академии наук УССР Л. А. Кульского, действие «серебряной» воды (при одинаковых концентрациях) значительнее действия хлора, хлорной извести, гипохлорида натрия и других сильных окислителей. По научным данным, всего 1 мг/л. серебра в течение 30 мин вызывал полную инактивацию вирусов гриппа А, В, Митре и Сендай. Уже при концентрации 0,1 мг/л серебро обладает выраженным фунгицидным действием.
«Серебряная» вода обладает бактерицидными свойствами при достаточно высоких концентрациях серебра, но при низких концентрациях серебро оказывает только бактериостатическое действия.
Однако, выбирая серебро в качестве обеззараживающего вещества, обязательно нужно помнить, что серебро – тяжелый металл. Как и другие тяжелые металлы, серебро способно накапливаться в организме и вызывать заболевания (аргироз – отравление серебром). В соответствии с СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества» допускается содержание в воде серебра не более 0,05 мг/л и СанПин 2.1.4.1116 – 02 «Питьевая вода. Гигиенические требования к качеству воды, расфасованной в емкости. Контроль качества» – не более 0,025 мг/л.
Многие потребители по старинке сутками настаивают воду в доморощенных серебряных водных фильтрах, в емкостях с монетами, ложечками и украшениями, и действительно «серебряная» вода может храниться годами. Но что кроется за таким способом очистки воды от микроорганизмов?
«Серебряная» вода обладает бактерицидными свойствами, при достаточно высоких концентрациях серебра, около 0,015 мг/л. При низких концентрациях (10 -4 … 10 -6 мг/л.), серебро оказывает только бактериостатическое действия, т. е. останавливает рост бактерий, но не убивает их. Спорообразующие разновидности микроорганизмов к серебру практически нечувствительны. Поэтому настаивание воды по старинке в доморощенных серебряных водных фильтрах, в емкостях с монетами, ложечками и украшениями не является гарантированным способом её обеззараживания.
Изложенные выше факты, таким образом, несколько ограничивают применение серебра. Оно может быть уместно только в целях сохранения исходно чистой воды для длительного хранения (например, на космических кораблях, в походах или при розливе бутилированной питьевой воды). Серебрение картриджей на основе активированного угля используют в бытовых фильтрах. Это делается с целью предотвращения обрастания фильтров микроорганизмами, так как отфильтрованные органические вещества являются хорошей питательной средой для многих бактерий.
5.1.3. Механизм воздействия
Сегодня существуют многочисленные теории, объясняющие механизм действия серебра на микроорганизмы. Наиболее распространенная – адсорбционная теория, в соответствии с которой клетка теряет жизнеспособность в результате взаимодействия электростатических сил, возникающих между клетками бактерий, имеющих отрицательный заряд, и положительно заряженными ионами серебра при адсорбции последних бактериальной клеткой.
Вораз и Тоферн (1957 г.) объясняли антимикробное действие серебра выведением из строя ферментов, содержащих SH - и СООН - группы, а K. Тонли, H. Вилсон – нарушением осмотического равновесия.
По другим теориям, происходит образование комплексов нуклеиновых кислот с тяжелыми металлами, вследствие чего нарушается стабильность ДНК и, соответственно, жизнеспособность бактерий.
Существует противоположное мнение, что серебро не оказывает прямого воздействия на ДНК клеток, а влияет косвенно, увеличивая количество внутриклеточных свободных радикалов, которые снижают концентрацию внутриклеточных активных соединений кислорода. Также допускают, что одной из причин широкого противомикробного действия ионов серебра является ингибирование трансмембранного транспорта Nа + и Cа ++ .
На основании данных механизм действия серебра на микробную клетку следующий: ионы серебра сорбируются клеточной оболочкой, которая выполняет защитную функцию. Клетка еще остается жизнеспособной, но при этом нарушаются некоторые ее функции – например, деление (бактериостатический эффект). Как только серебро адсорбировалось на поверхности микробной клетки, оно проникает внутрь её, угнетает ферменты дыхательной цепи, а также разобщает процессы окисления в микробных клетках, в результате чего клетка гибнет.
Коллоидное серебро – продукт, состоящий из микроскопических частиц серебра, взвешенных в деминерализованной и деионизированной воде. Коллоидное серебро, которое получают электролитическим методом, естественный антибиотик, разрешенный к применению в США Федеральной комиссией по питанию и медикаментам еще в 1920 г. Эффективность бактерицидного действия коллоидного серебра объясняется его способностью подавлять работу фермента, с помощью которого обеспечивается кислородный обмен чужеродных простейших микроорганизмов, поэтому они и погибают из-за нарушения снабжения кислородом, необходимого для их жизнедеятельности.
5.1.4. Аппаратурное оформление
Приготовить «серебряную» воду в домашних условиях возможно, но не эффективно. Можно настаивать воду в серебряном сосуде, погрузить в емкость с водой серебряные предметы, украшения и т. п… В настоящее время «серебряную» воду производят в электрических приборах – ионаторах. Принцип действия ионатора серебра основан на электролитическом методе. Конструктивно прибор состоит из электролизера с серебряными электродами (серебро Ср 99,99) и блока питания, подключаемого к сети постоянного тока. При пропускании постоянного тока через погруженные в воду серебряные (или серебряно-медные) электроды серебряный электрод (анод), растворяясь, насыщает воду ионами серебра. Концентрация полученного раствора при заданной силе тока зависит от времени работы источника тока и объема обрабатываемой воды. Если грамотно подобрать ионатор, то остаточное содержание растворённого в воде серебра не превысит предельной дозы 10 -4 …10 -5 мг/л (при этом в контактном слое серебрения воды концентрации могут достигать значения 0,015 мг/л), что позволяет осуществлять одновременно бактерицидную и бактериостатическую обработку воды. В табл. 4 приведены условия получения «серебряной» воды на примере ионатора «ЛК-41» (источник питания ионатора – элекотросеть переменного тока напряжением 220 В, ток нагрузки, мА 0±20 %, масса серебра, переводимого ионатором в водный раствор за 1 минуту, мг 0,4±20 %, температура обрабатываемой воды от 1 до 40 °С).
Таблица 4
Готовые растворы серебра необходимо хранить в темном месте или в непрозрачной закрытой посуде, так как на свету ионы серебра восстанавливаются до металла, раствор темнеет, а серебро – выпадает в осадок.
Начало выпуска ионаторов в России относится к далекому 1939 г, когда началось серийное производство стационарных ионаторов, переносных и дорожных серий ЛК. Производство продолжается и сейчас.
Сейчас на российском рынке представлены ионаторы разных производителей и конструктивного исполнения, с электронным управление и самые простые автономные карманные: «Невотон ИС», «Пингвин», «Сильва», «Дельфин», «ЛК», «Акватай» и др.
При работе ионатора на серебряных пластинах выделяется распыленное серебро черного цвета, которое на качество приготавливаемого раствора не влияет. В растворе серебра после отключения ионатора процесс уничтожения бактерий происходит не сразу, а в течение времени, указанного в графе время выдержки.
5.1.5. Применение активных углей и катионитов, насыщенных серебром
В настоящее время активированный уголь используется во многих процессах очистки воды, пищевой промышленности, в процессах химических технологий. Основное назначение угля – это адсорбции органических соединений. Именно отфильтрованные органические вещества являются идеальной питательной средой для размножения бактерий при остановке движения воды. Нанесение серебра на активированный уголь препятствует росту бактерий внутри фильтра благодаря бактерицидным свойствам этого металла. Технология нанесения серебра на поверхность угля уникальна тем, что серебро не смывается с поверхности угля в процессе фильтрования. В зависимости от производителя, вида исходного сырья, марки угля на поверхность наносят 0,06–0,12 % массовых серебра.
На российском рынке представлены активированные угли с нанесенным серебром производителей: С-100 Ag или С-150 Ag фирмы Purolite; AGС производится на базе активированного угля 207С компанией Chemviron Carbon; российские производители предлагают УАИ-1, изготавливаемый из древесного активного угля БАУ-А; угли марки КАУСОРБ-213 Ag и КАУСОРБ-222 Ag получены из активных углей марок КАУСОРБ-212 и КАУСОРБ-221 и т. д.
Несмотря на достаточно высокую эффективность олигодинамии в целом, нельзя говорить об абсолютной универсальности этого способа. Дело в том, что целый ряд вредных микроорганизмов оказывается вне зоны его действия – многие грибы, бактерии (сапрофитные, спорообразующие). Тем не менее пропущенная через такой фильтр, вода обычно долго сохраняет свои бактерицидные свойства и чистоту.
5.2. Медь
Медь – химический элемент, обозначается символом Сu. Название элемента происходит от названия острова Кипр (лат. Cuprum), на котором изначально добывали медь. Имеет порядковый номер 29, атомный вес – 63,546, валентность – I, II, плотность – 8,92 г/см 3 , температура плавления – 1083,4 °С, кипения – 2567 °С.
Медь – мягкий, ковкий металл красного цвета, обладает высокой тепло– и электропроводностью (занимает второе место по электропроводности после серебра).
Медь встречается в природе как в различных соединениях, так и в самородном виде. Существуют различные сплавы меди, самые известные из них латунь – сплав с цинком, бронза – сплав с оловом, мельхиор – сплав с никелем и др., как присадка медь присутствует в баббитах.
Медь широко распространена в электротехнике (из-за ее низкого удельного сопротивления) для изготовления силовых кабелей, проводов или других проводников, например, при печатном монтаже. Ее широко применяют в различных теплообменниках, к которым относятся радиаторы охлаждения, кондиционирования и отопления из-за очень важного свойства меди – высокой теплопроводности.
Некоторые соединения меди могут быть токсичны при превышении предельно допустимых концентраций в пище и воде. Содержание меди в питьевой воде также регламентируется СанПиН 2.1.4.1074-01 и не должно превышать 2 мг/л. Лимитирующий признак вредности вещества, по которому установлен норматив, – санитарно-токсикологический.
Уровень меди в питьевой воде обычно достаточно низкий и составляет несколько микрограмм на литр. Ионы меди придают воде отчётливый «металлический вкус». Порог чувствительности органолептического определения меди в воде составляет приблизительно 2–10 мг/л.
5.2.1. История
Об антибактериальных свойствах меди известно очень давно. В древней Руси для медицинских целей применяли, так называемую, «колокольную» воду. Получали её во время литья колоколов, когда еще раскаленную отливку остужали в емкостях, наполненных водой. Колокола отливали из бронзы – сплава меди и олова, а для улучшения их звучания в этот сплав добавляли серебро. За время остывания вода обогащалась ионами меди, олова и серебра.
Совместное действие ионов меди и серебра превосходит силу «серебряной» воды, даже если в последней концентрация ионов серебра в несколько раз выше. Важно понимать, что даже «колокольная» вода, если ее применять бесконтрольно, может нанести большой вред организму.
Медь и ее сплавы иногда применяют для местного обеззараживания воды, чаще для обеззараживания в бытовых и походных условиях, обогащая воду ионами меди.
Издревле было также замечено, что вода, хранящаяся или перевозимая в медных сосудах, была, более высокого качества и долго не портилась, в отличие от воды, содержащейся или перевозимой в сосудах из других материалов (в такой воде не происходило видимого образования слизи).
Существует огромное количество исследовательских работ, подтверждающих бактерицидные свойства меди.
5.2.2. Механизм воздействия
Исследования по выяснению механизма антибактериального действия меди проводили еще в давние времена. Например, в 1973 г. ученые из лаборатории «Колумбус Баттел» провели всесторонний научный и патентный поиск, в котором собрали всю историю исследования бактериостатических и дезинфицирующих свойств меди и поверхностей медных сплавов за период 1892–1973 гг.
Было сделано открытие, а в дальнейшем подтверждено, что поверхности медных сплавов обладают особым свойством – уничтожать широкий спектр микроорганизмов.
Последние 10 лет интенсивно проводились исследования по воздействию меди на возбудителей внутрибольничных инфекций: кишечной палочки, метициллин-устойчивой формы золотистого стафилококка (MRSA), вируса гриппа А, аденовируса, патогенных грибков и пр. Исследования, проводимые в Америке, показали, что поверхность медного сплава (зависит от марки сплава) способна убить кишечную палочку через 1–4 ч контакта, при этом популяции кишечной палочки погибают на 99,9 %, в то время как, например, на поверхности из нержавеющей стали микробы могут выживать в течение недели.
Латунь, из которой часто делают дверные ручки и нажимные пластины, тоже обладает бактерицидным эффектом, но для этого требуется более продолжительное время экспозиции, чем для чистой меди.
В 2008 г. после длительных исследований Федеральное агентство по охране окружающей среды США (US ЕРА) официально присвоило меди и её нескольким сплавам статус материала, обладающего бактерицидной поверхностью.
5.2.3. Аппаратурное оформление
Медь и ее сплавы иногда применяют для местного обеззараживания воды (если нет других, более подходящих способов и реактивов, дающих гарантированный обеззараживающий эффект). Чаще ее применяют для обеззараживания воды в бытовых и походных условиях, обогащая воду ионами меди.
На рынке представлено несколько типов ионаторов – устройств, использующих принцип гальванической пары и электрофореза. В качестве второго электрода, обеспечивающего разность потенциалов, используется золото. При этом золото тонким слоем наносится на специальную подложку электрода, полностью делать электрод из одного золота не имеет смысла, поэтому внутренняя часть электрода изготавливается из сплава меди и серебра в определенном соотношении, как правило, сплав 17/1. Конструктивно это может быть простая пластина из медно-серебряного сплава (17/1) с вкраплениями золота, или более сложный прибор проточного типа с микроконтроллерным устройством управления.
6. Ультрафиолетовое обеззараживание
6.1. Описание метода
Электромагнитное излучение в пределах длин волн от 10 до 400 нм называется ультрафиолетовым.
Для обеззараживания природных и сточных вод используют биологически активную область спектра УФ-облучения с длиной волны от 205 до 315 нм, называемую бактерицидным излучением. Наибольшим бактерицидным действием (максимум вирулицидного действия) обладает электромагнитное излучение на длине волны 200–315 нм и максимальным проявлением в области 260±10 нм. В современных УФ-устройствах применяют излучение с длиной волны 253,7 нм.
а – кривая бактерицидного действия ультрафиолета б – кривая бактерицидного действия ультрафиолета и спектры поглощения ДНК и протеина
Метод УФ-дезинфекции известен с 1910 г., когда были построены первые станции для обработки артезианской воды во Франции и Германии. Бактерицидное действие ультрафиолетовых лучей объясняется происходящими под их воздействием фотохимическими реакциями в структуре молекулы ДНК и РНК, составляющими универсальную информационную основу механизма воспроизводимости живых организмов.
Результат этих реакций – необратимые повреждения ДНК и РНК. Кроме того, действие УФ-излучения вызывает нарушения в структуре мембран и клеточных стенок микроорганизмов. Всё это в конечном итоге приводит к их гибели.
Механизм обеззараживания УФ-облучением основан на повреждении молекул ДНК и РНК вирусов. Фотохимическое воздействие предполагает разрыв или изменение химических связей органической молекулы в результате поглощения энергии фотона. Имеют место также вторичные процессы, в основе которых лежит образование в воде под действием УФ-облучения свободных радикалов, которые усиливают вирулицидный эффект.
Степень инактивации или доля погибших под воздействием УФ-излучения микроорганизмов пропорциональна интенсивности излучения и времени воздействия.
Произведение интенсивности излучения и времени называется дозой облучения (мДж/см 2) и является мерой вирулицидной энергии. Из-за различной сопротивляемости микроорганизмов доза ультрафиолета, необходимая для их инактивации на 99,9 %, сильно варьируется от малых доз для бактерий до очень больших доз для спор и простейших.
Схема установки для УФ-обеззараживания воды
6.2. Доза излучения
Основными факторами, влияющими на эффективность обеззараживания природных и сточных вод УФ-облучением, являются:
– чувствительность различных вирусов к действию УФ-облучения;
– мощность лампы;
– степень поглощения УФ-облучения водной средой;
– уровень взвешенных веществ в обеззараживаемой воде.
Различные виды вирусов при одинаковых условиях облучения различают по степени чувствительности к УФ-облучению. Дозы облучения, необходимые для инактивации отдельных видов вирусов на 99,0–99,9 %, приведены в табл. 5.
Таблица 5
(Информация приведена по данным МУК 43.2030-05 «Санитарно-вирусологический контроль эффективности обеззараживания питьевых и сточных вод УФ-облучением»).
При прохождении через воду УФ-излучение ослабевает вследствие эффектов поглощения и рассеивания. Степень поглощения определяется физико-химическими свойствами обрабатываемой воды, а также толщиной её слоя. Для учёта этого ослабления вводится коэффициент поглощения водой


